《威士忌生产工艺与营销策略(第二版)》第十四章
第14章:威士忌分析
Ross Aylott
摘要
- 威士忌含有数百种微量化合物(同系物),这些化合物源于发酵过程中使用的原材料以及后续的蒸馏和陈酿工艺。这些同系物赋予威士忌独特的感官特征。对它们的分析是现代发酵和蒸馏过程控制、工艺研究与开发、产品质量保证以及品牌保护的组成部分。尽管各种形式的色谱法是提供广泛定性和定量数据的理想选择,但其他仪器技术正在提供新的见解,有助于在全球范围内维护威士忌的质量、真实性和声誉。
关键词
分析 真实性 色谱法 成分 同系物 定义 标签 质量保证
引言
-
近几十年来,我们对威士忌的分析认知迅速扩展。从20世纪60年代气相色谱法(Duncan和Philp,1966;Singer和Styles,1965)、气相色谱-质谱法(GC-MS)(Kahn,1969)的引入开始,随后是高效液相色谱法(HPLC)(Lehtonen,1983a)和离子交换色谱法。已知威士忌中含有数百种同系物,包括醇类、酸类、酯类、羰基化合物、酚类、烃类以及含氮和含硫化合物(Swan等人,1981)。使用壶式蒸馏器蒸馏的威士忌比在连续蒸馏器中经过更高精馏的威士忌含有更丰富的同系物。同系物浓度通常从高百万分之几(mg/L)到低十亿分之几(μg/L)不等。
-
同系物是生产过程的天然成分。有些明显贡献了感官特征,有些则不然。然而,所有同系物共同帮助使每种威士忌独一无二。每种同系物的存在都与生产过程的特定环节相关——例如使用的谷物以及发酵、蒸馏和陈酿过程。这些过程影响最终产品中每种同系物的浓度。发酵中形成的高级醇等同系物可能在蒸馏过程中通过精馏降低浓度甚至消除。发酵中形成的乙酯可能在陈酿过程中浓度增加。与木材相关的同系物在蒸馏结束时不存在,而是在陈酿期间从木桶中提取到液体中。
世界威士忌及其监管定义
蒸馏酒行业中的威士忌
- 大多数国家的法律中都有关于威士忌的定义。这些法律有助于保护消费者利益、制造商业务以及国家税收收入。最重要的定义来自特定威士忌的原产国。许多其他国家要么在自己的法规中引用原产国的定义,要么使用源自原产国定义的词汇和短语。以下部分概述了威士忌/whiskey的定义,特别是其原产国的威士忌定义。
欧盟的威士忌
- 欧盟委员会第110/2008号法规对威士忌/whiskey以及另外46类蒸馏酒进行了定义,取代了早期的委员会法规1576/89/EEC(EEC,1989)。该法规规定:
(a) 威士忌或whiskey是一种蒸馏酒,仅通过以下方式生产:
(i) 对由发芽谷物制成的 mash 进行蒸馏,可添加或不添加其他谷物整粒,且该mash已:
— 通过其中所含麦芽的淀粉酶进行糖化,可添加或不添加其他天然酶,
— 通过酵母的作用进行发酵;
(ii) 以低于94.8%(体积比)的酒精度进行一次或多次蒸馏,使蒸馏液具有源自所用原材料的香气和味道;
(iii) 最终蒸馏液在容量不超过700升的木桶中陈酿至少三年。
最终蒸馏液仅可添加水和纯焦糖(用于着色),并保留源自第(i)、(ii)和(iii)点所述生产过程的颜色、香气和味道。
(b) 威士忌或whiskey的最低体积酒精度为40%。
© 不得添加附件I(5)所定义的酒精,无论是否稀释。
(d) 威士忌或whiskey不得加糖或调味,除用于着色的纯焦糖外,不得含有任何添加剂。
法规110/2008的附件III列出了欧盟生产的主要威士忌的五个地理标志,包括“苏格兰威士忌”、“爱尔兰威士忌”、“西班牙威士忌”、“布列塔尼威士忌”和“阿尔萨斯威士忌”(后两者均来自法国)。后文描述的国家法规对苏格兰和爱尔兰威士忌的定义进行了细化。
美国的威士忌
- 美国联邦法规(27 CFR 5.22-身份标准)中记录了威士忌及其他蒸馏酒的身份标准:
威士忌是一种从谷物发酵mash中蒸馏出的酒精蒸馏液,以低于190度proof的方式生产,使蒸馏液具有通常归因于威士忌的味道、香气和特征,存储在橡木容器中,并以不低于80度proof装瓶…
尽管威士忌的标准很直接,但这些标准继续定义了美国生产的各种类型的whiskey,后文将讨论这些类型。美国的身份标准还通过参考每个生产国的特定法律来定义苏格兰、爱尔兰和加拿大威士忌;更多细节可在第5章中找到。
苏格兰威士忌
- 苏格兰威士忌仅在苏格兰使用谷物、酵母和水制成。苏格兰威士忌有两种类型:麦芽威士忌和谷物威士忌。苏格兰麦芽威士忌由大麦芽发酵制成,所得酒精通过铜制壶式蒸馏器分批蒸馏浓缩。苏格兰谷物威士忌由包含其他未发芽熟谷物(如大麦、小麦或玉米)和较小比例大麦芽的mash发酵制成。所得酒精通过连续蒸馏工艺浓缩,最常见的设计是科菲或专利蒸馏器。然后,麦芽和谷物新制烈酒均用水稀释至约65-70%(体积比)酒精度,并在橡木桶中陈酿至少3年。陈酿结束后,威士忌要么进行调配,要么作为单一蒸馏厂产品,再用水进一步稀释,以最低40%(体积比)酒精度装瓶。
苏格兰威士忌在英国法律《2009年苏格兰威士忌法规》(SWA,2009)中有定义。与1988年《苏格兰威士忌法案》下制定的早期《1990年苏格兰威士忌令》相比,该最新法规取代并设定了更严格的标准。英国和欧盟法规均定义了生产过程,但未定义分析参数(除了最大蒸馏酒精度和最低装瓶酒精度)。《2009年苏格兰威士忌法规》内容如下:
1 | |
爱尔兰威士忌
- 与苏格兰一样,爱尔兰也使用发芽和未发芽谷物的混合物生产麦芽和谷物威士忌,但与苏格兰威士忌不同的是,在糖化过程中可以使用外源性淀粉分解酶。爱尔兰麦芽威士忌在三个壶式蒸馏器中进行三次蒸馏,爱尔兰谷物威士忌在三柱系统中连续蒸馏,使其特征比许多苏格兰同类产品更清淡。与苏格兰威士忌一样,爱尔兰威士忌的最低陈酿期为三年。生产和陈酿可在爱尔兰或北爱尔兰进行,目前可在科克和邓多克附近(爱尔兰)以及布什米尔斯(北爱尔兰)找到。法律定义可在《1980年爱尔兰威士忌法案》中找到,其地理标志列于欧盟法规110/2008的附件III中。更多细节可在第2章中找到。
美国威士忌
- 如前所述,蒸馏酒的身份标准记录在美国联邦法规中。特别是,波本威士忌是:
在美国以不超过80%(体积比)酒精度(160 proof)从不少于51%玉米的发酵mash中生产的威士忌,并以不超过62.5%(体积比)酒精度(125 proof)存储在新的炭化橡木容器中。
陈酿两年或更长时间的威士忌进一步指定为“纯”—例如,“纯波本威士忌”。田纳西威士忌是在田纳西州生产的纯波本威士忌。更多细节在第5章中提供。
加拿大威士忌
- 加拿大威士忌在加拿大《食品和药物法案》(1993)中有定义。
加拿大威士忌、加拿大黑麦威士忌和黑麦威士忌
(a) 应—
(i) 为可饮用的酒精蒸馏液,或可饮用酒精蒸馏液的混合物,从谷物或谷物产品的mash中获得,该mash通过麦芽的淀粉酶或其他酶糖化,并通过酵母或酵母与其他微生物的混合物发酵。
(ii) 在加拿大的小木桶中糖化、蒸馏和陈酿不少于三年。
(iii) 具有通常归因于加拿大威士忌的味道、香气和特征,并且
(iv) 根据《消费税法案》及其下制定的法规制造;并且
(b) 可包含焦糖和调味料。
其他国家
- 其他国家遵循类似的监管主题。日本的威士忌法规(见第3章)包含对谷物和最低蒸馏酒精度的要求。中国的标准(PRC,2008)也要求使用谷物,并将威士忌定义为“由麦芽和谷物通过糖化、发酵、蒸馏、陈酿和调配制成的蒸馏酒”。澳大利亚和新西兰也要求威士忌由谷物制成。(有关印度威士忌生产和使用甘蔗的详细信息,请参见第4章。)
威士忌的成分与分析
- 如前所述,威士忌含有数百种同系物(Kahn,1969;Maarse和Visscher,1985a,b;Swan等人,1981),其分析目的广泛,从研究和工艺改进到日常生产质量保证。如今,除了酒精度测量和某些工艺监测技术外,威士忌分析师主要依赖气相色谱和液相色谱作为首选分析技术。与许多它所取代的老式比色法和滴定法相比,色谱法在选择性、灵敏度和速度方面具有优势。大多数知名的色谱检测器都有其作用,从气相色谱的火焰离子化到质谱检测,以及液相色谱的紫外到荧光检测。样品制备已尽可能简化,并且在可能的情况下使用在适当内标存在下直接进样威士忌样品的方法。本节概述了当前可用的方法、使用背景和获得的典型结果。
酒精度测量
-
酒精度测量是威士忌生产中的关键定量测量,因为它有助于衡量整个碳水化合物转化过程的效率,确定向政府缴纳的消费税,并确保消费者获得产品标签上声明的酒精度。酒精度通常定义为特定温度下溶液中乙醇的体积浓度。酒精浓度通常以百分比或proof度表示,其中100%(体积比)的纯酒精相当于200°美国proof度。酒精度测定方法发表于AOAC国际分析官方方法(Horwitz,2000)和欧盟第2870号法规(2000)关于“蒸馏酒分析的共同体参考方法”。
-
使用两种测量版本:实际酒精度和表观酒精度。实际酒精度是测试样品蒸馏液中乙醇的体积百分比,其中所有溶解固体均已去除,这给出了真实结果。表观酒精度是未经事先蒸馏的测试液体中乙醇的体积百分比,其真实结果被溶解固体所掩盖。溶解固体的存在增加了样品的密度,导致表观酒精度测量值低于相应的实际酒精度测量值。实际酒精度与表观酒精度之间的差异称为“模糊度”:
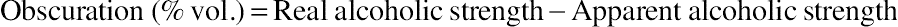
-
大多数威士忌中的溶解固体量较低。在苏格兰威士忌中,模糊度通常<0.2%(体积比);因此,出于税收或贸易目的进行强度测量之前,通常不需要蒸馏。美国酒精、烟草和火器管理局(ATF)法规要求,当溶解固体超过600 mg/100 mL时,在测量酒精度之前对样品进行蒸馏。当溶解固体在400至600 mg/100 mL之间时,模糊度会添加到确定的proof度中(联邦法规法典,1998b)。
-
酒精度测量通常基于溶液的密度。纯乙醇在20°C时的密度为789.24 kg/m³,而水在20°C时的密度为998.20 kg/m³。乙醇/水混合物的密度将介于这两个值之间;密度越低,酒精度越高。基于液体密度的三种主要技术涉及使用比重计、比重瓶和电子密度计。
-
在生产环境中,比重计传统上是酒精度测量的首选方法。比重计是一种经过校准的加权装置,漂浮在测试液体中,其深度对应于液体的密度。读数取液体与比重计刻度相交的位置。根据所用的比重计和测试液体的体积,测量精度通常可达±0.1%(体积比)。
-
使用比重瓶和电子密度计可获得更精确的酒精度测量值。比重瓶是一种小型(通常为Pyrex®玻璃)容器,典型体积为100 mL,用于确定测试液体的比重或密度。然后从表格中读取酒精度,该表格给出了作为水/酒精混合物密度函数的体积酒精度。国际法制计量组织(OIML)已为此采用了国际表格。该程序需要高度熟练且缓慢,但精度至少为±0.1%(体积比),需要精确的温度控制和测量。
-
在20世纪80年代,电子密度计成为实验室、大型蒸馏厂和装瓶厂中酒精度测定的首选方法。测量基于样品在振荡池中的共振频率振荡。池的振荡频率因测试样品的附加质量而改变,这可用于确定其密度和相应的酒精度。需要小测试体积(<5 mL),精度可达±0.1%(体积比)。一旦校准,仪器稳定且可自动化。商业仪器由Anton Paar GmbH(奥地利格拉茨)和京都电子制造有限公司(日本京都)制造。
-
最近,近红外光谱已应用于模糊液体的实际酒精度测量。这种使用Infratec™(丹麦Foss)开发的方法消除了分析前蒸馏的需要,特别适用于威士忌基利口酒和低强度即饮配方等模糊液体的酒精度测量。
-
最后,气相色谱可用于分离测试液体中的乙醇特定峰,从中可以计算实际酒精度。结果通常精确到±1%(体积比)。该方法可以自动化,但精度不足以用于税收目的。
主要挥发性同系物
-
除乙醇外,威士忌中的主要同系物是高级醇,即正丙醇、异丁醇以及2-和3-甲基丁醇。关于各种蒸馏酒中这些同系物的大量有用工作已发表(Duncan和Philp,1966;Kahn,1969;Shoeneman和Dyer,1973)。这些同系物的气相色谱分析通常还包括甲醇、乙醛和乙酸乙酯的分离。所有这些同系物都是在发酵过程中形成的,它们的最终浓度受蒸馏和调配过程的影响。主要挥发性同系物在mg/L(ppm)水平下通过一次直接进样气相色谱分离进行分析,使用填充柱或毛细管柱上的极性固定相(Martin等人,1981)。常见的内标包括1-或3-戊醇,该方法已通过全面的实验室间试验验证(Kelly等人,1999)。
-
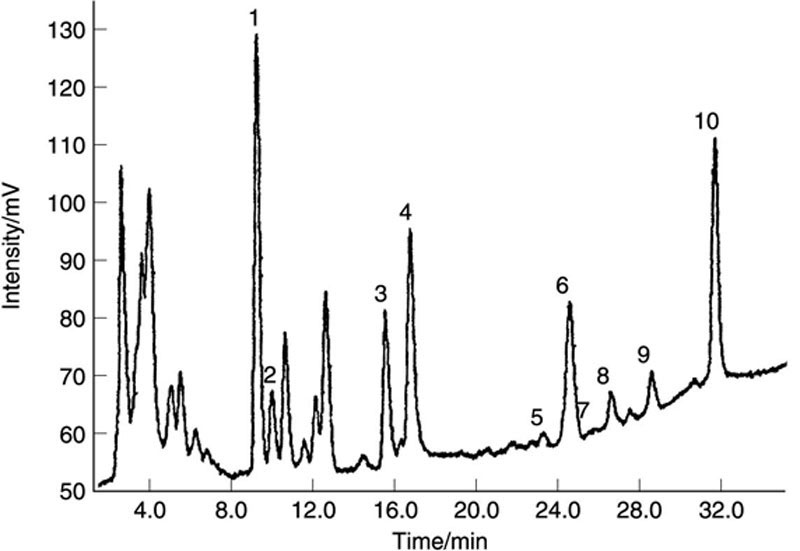
调和苏格兰威士忌的典型高级醇色谱图如图14.1所示(使用Carbowax® 20M在Carbopak® B上作为固定相),定量结果见表14.1。结果表明,来自连续科菲蒸馏器蒸馏的苏格兰谷物威士忌几乎不含在异丁醇之后洗脱的同系物,而来自双壶式蒸馏器蒸馏的苏格兰麦芽威士忌在异丁醇之后洗脱的低挥发性同系物要丰富得多。低挥发性同系物,特别是2-和3-甲基丁醇,在科菲蒸馏器的精馏段从谷物烈酒中去除,并作为杂醇油回收。调和苏格兰和爱尔兰威士忌的同系物谱代表了其调配中使用的各种麦芽和谷物威士忌。波本威士忌富含同系物,因为波本蒸馏过程中除了双重蒸馏器中的啤酒蒸馏器外,几乎没有精馏。与所检查的其他威士忌相比,加拿大威士忌作为谷物中性烈酒和波本风格蒸馏液的混合物,同系物浓度相对较低。在此分析中可能检测到的其他痕量同系物还包括正丁醇和乙酸。
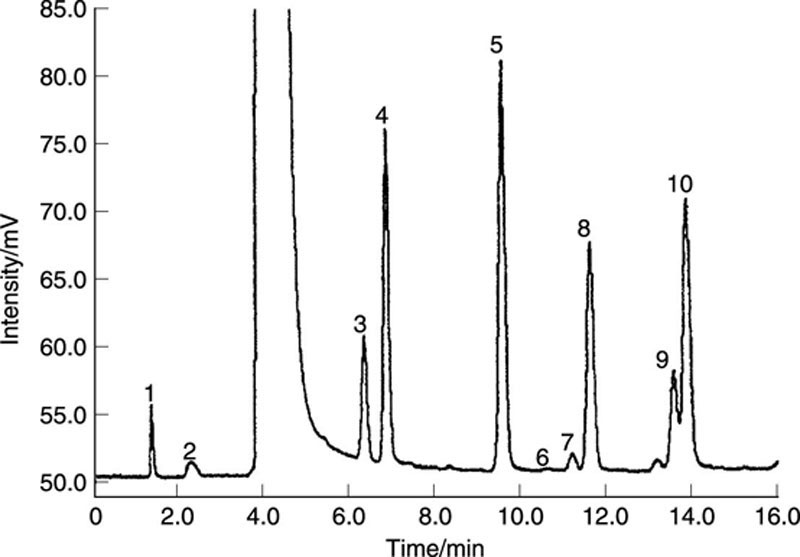
| 威士忌类型 | 乙醛 | 甲醇 | 乙酸乙酯 | 正丙醇 | 异丁醇 | 2-甲基丁醇 | 3-甲基丁醇 | 2-和3-甲基丁醇 | 比率1 | 比率2 |
|---|---|---|---|---|---|---|---|---|---|---|
| 苏格兰麦芽威士忌 | 17 | 6.3 | 45 | 41 | 80 | 62 | 114 | 176 | 2.2 | 2.8 |
| 苏格兰谷物威士忌 | 12 | 8.5 | 18 | 72 | 68 | 8 | 15 | 23 | 0.3 | 2.8 |
| 苏格兰调和威士忌 | 5.4 | 8.9 | 23 | 55 | 62 | 26 | 46 | 72 | 1.2 | 2.8 |
| 爱尔兰威士忌 | 4.1 | 10 | 13 | 28 | 15 | 18 | 32 | 49 | 3.1 | 2.8 |
| 肯塔基波本威士忌 | 15 | 17 | 89 | 28 | 160 | 143 | 242 | 385 | 2.4 | 2.7 |
| 加拿大威士忌 | 3.3 | 7.9 | 7.1 | 6.2 | 6.9 | 7 | 9 | 16 | 2.3 | 2.2 |
-
比率1 = 2-和3-甲基丁醇/异丁醇。
-
比率2 = 3-甲基丁醇/2-甲基丁醇。
-
威士忌同系物分析中使用的正常浓度单位是g/100 L绝对酒精(LAA)。因此,同系物浓度与纯酒精的体积相关,而不仅仅是样品液体的体积。这个浓度单位乍看起来很奇怪,但事实证明非常有用,因为它可以关联到威士忌在制造过程中可能出现的许多不同酒精度。例如,苏格兰谷物烈酒可能在约94.6%的酒精度下蒸馏,在65%的酒精度下陈酿,调配、稀释,最后以40%(体积比)的酒精度装瓶。
-
主要挥发性同系物分析是应用于威士忌的最广泛使用的气相色谱方法,并在产品的整个生命周期中找到应用。例如,它可用于监测用于蒸馏苏格兰谷物烈酒和加拿大谷物中性烈酒(GNS)的连续蒸馏器中精馏的效率,用于竞争对手产品分析以确定调和苏格兰威士忌中麦芽威士忌的百分比,以及用于消费者保护活动以确认品牌真实性。色谱学前时代的分光光度法和滴定法(Shoeneman和Dyer,1973;Singer和Styles,1965)现在几乎已过时,仅偶尔需要用于支持过时的法规要求。当通过这些较旧的方法测定总酯时,总酯含量的50%以上是乙酸乙酯。同样,主要的挥发性酸归因于乙酸。如果需要,总醛、酯、杂醇油、糠醛、颜色和提取物的方法可以在AOAC国际分析官方方法(Horwitz,2000)和饮用烈酒分析方法(饮用烈酒分析研究委员会,1979)中找到。
痕量同系物
- 接下来的主要同系物组是低浓度和亚mg/L水平的长链烷基醇、醛和酯。其中一些同系物以较高浓度存在,可以通过填充柱程序升温极性柱(如Chromosorb® B上的Carbowax® 20M)直接进样测定。然而,最好的分离是在极性毛细管柱上使用测试液体的有机溶剂萃取物实现的。氯化氟碳化合物(CFCs)是理想的萃取溶剂,直到它们因环境原因停止使用。戊烷也是一种良好的萃取溶剂(用1 mL戊烷萃取10 mL样品)。典型调和苏格兰威士忌萃取物的毛细管柱色谱图如图14.2所示。
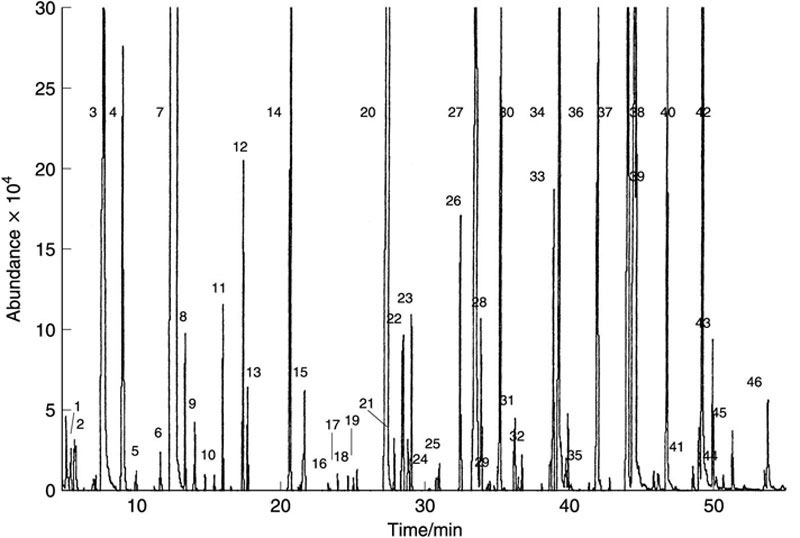
-
毛细管柱系统可以使用汽化不分流和柱上进样。固相微萃取(SPME)已发展成为毛细管柱分析前可靠且简单的样品制备方法(Lee等人,2001)。这些高分辨率分离通常与质谱检测相关联,质谱仪在电子轰击模式下运行。该技术已应用于爱尔兰和苏格兰威士忌(Fitzgerald等人,2000)。
-
感官分析在第13章中介绍。许多痕量同系物与特定风味特征相关联(Lee等人,2001),本章中描述的方法与它们的分析相关。
陈酿同系物
-
分子水平上的威士忌陈酿涉及同系物添加、同系物减少和同系物生成的过程(Philp,1986)。在这些过程中,新制烈酒(新蒸馏液)的刺鼻和 harsh 特征减弱,成熟威士忌的更顺滑、更复杂的特征得以发展。
-
苏格兰和爱尔兰威士忌陈酿桶通常由西班牙和美国橡木制成。波本威士忌桶仅由新的炭化美国橡木制成,且仅使用一次。这导致二手美国橡木桶市场繁荣,加拿大和苏格兰威士忌行业是主要买家。苏格兰和爱尔兰的陈酿仓库往往全年凉爽,而美国的仓库夏季可能炎热,冬季寒冷。一些波本威士忌公司在冬季加热仓库以加速陈酿过程。随着烈酒特征的发展,由于蒸发(被爱好者称为“天使的份额”),每个桶中的体积每年减少1%至2%。
-
同系物添加过程是通过乙醇与木材木质素的相互作用从橡木桶中提取到液体中的过程(Reazin,1979)。由此产生的同系物被称为木质素降解产物(LDPs)。多酚类物质通过高效液相色谱(HPLC)测定(Lehtonen,1983a,b),橡木内酯通过毛细管柱气相色谱测定。新制威士忌在陈酿开始前是清澈的液体,但在陈酿过程中会从橡木桶中获得不同量的颜色和炭化 wood 颗粒。
-
具有紫外和/或荧光检测的直接进样梯度洗脱反相HPLC是陈酿过程中最常用的分析类型(Aylott等人,1994)。该分析可用于定量LDPs,包括没食子酸、香草酸、丁香酸、香草醛、丁香醛、松柏醛、鞣花酸和东莨菪素,以及糠醛(存在于苏格兰麦芽烈酒中)和5-羟甲基糠醛(主要与烈酒焦糖相关)。典型的色谱图如图14.3所示。
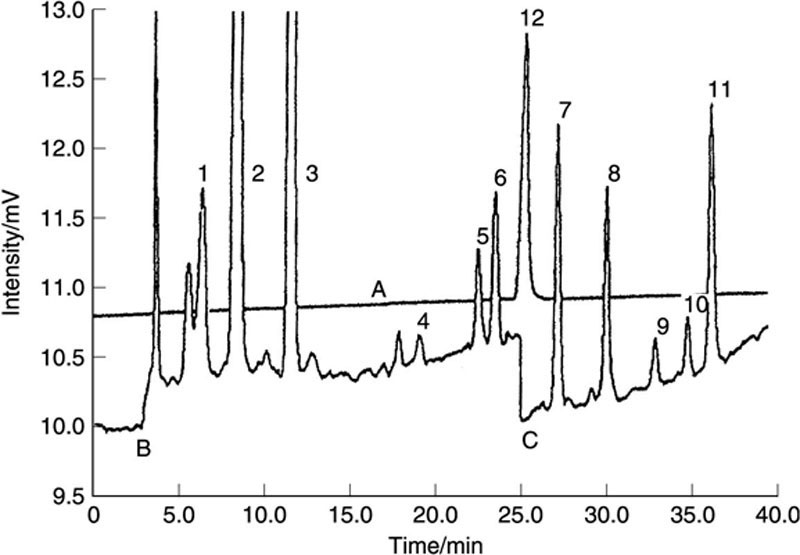
-
同系物减少过程涉及挥发(如二甲硫醚的损失)、吸附到炭化 wood 上以及羰基化合物的氧化。同系物生成过程涉及氧化形成缩醛、酯化形成更多酯类以及水解形成醌类。
-
含硫同系物如挥发性二甲硫醚(DMS)、二甲基二硫醚(DMDS)和低挥发性二甲基三硫醚(DMTS)可通过程序升温毛细管柱气相色谱结合火焰光度检测测定(Beveridge,1990)。DMTS是苏格兰麦芽威士忌中的重要风味化合物。这些超痕量化合物通过动态顶空浓缩技术从测试样品中浓缩到Chromosorb® 101上,然后进行热解吸、色谱分离和低μg/L水平的检测。
威士忌年龄
-
给定威士忌桶中橡木衍生同系物的浓度随陈酿时间增加。因此,有可能开始绘制同系物浓度与年龄的关系图。然而,使用的桶类型多种多样,从波本威士忌过程中使用的新炭化橡木(会产生相对较高浓度的添加陈酿同系物)到用于苏格兰谷物威士忌的第二或第三次 refill 桶(导致较少的同系物添加)。桶也可以重建和再生。这意味着基于陈酿同系物浓度的年龄确定是不精确的。然而,陈酿同系物的色谱图是一致的,并且在检查可疑产品中的虚假真实性声明时可能有用,其中怀疑使用了木材风味添加剂。最近的工作涉及使用近红外反射(NIR)作为加拿大威士忌陈酿的预测工具(Livermore,2012)。
-
大气二氧化碳中的天然¹⁴C通过新陈代谢被所有植物吸收,包括用于威士忌制造的谷物。1945年至1960年间(对应大气核试验的开始和结束),¹⁴C的自然水平有所上升(Baxter和Walton,1971),现在已回落至接近1945年前的水平。对从威士忌样品中浓缩的乙醇中¹⁴C水平的分析已被用于估计谷物生长的年份,然后将该年份与年龄相关联。分析精度有限,这显然降低了所得数据的准确性。
pH值、残留物、灰分、阴离子和阳离子
-
40%乙醇体积强度的威士忌的自然pH值通常在4至4.5的范围内。这种弱酸性是痕量有机酸的结果,其中乙酸是主要成分。pH计的校准溶液应在40%乙醇中制备。当用软化水而不是去离子水稀释至装瓶强度时,威士忌的pH值会更高。
-
威士忌残留物较低(通常<0.2 g/100 mL),通常代表陈酿过程中从桶中衍生的非蒸汽挥发性物质。此分析的样品在蒸汽浴上制备。灰分值低得多(通常<0.02 g/100 mL),代表测试样品在炉中干燥时残留的不挥发无机化合物。灰分将包括痕量金属如钙、镁、钠和钾(均通常处于低mg/L水平),它们源自威士忌过程中使用的水和桶。这些痕量金属可通过火焰原子化原子吸收光谱法或电化学检测离子色谱法直接在威士忌中分析。
-
还存在各种痕量糖,它们源自桶提取物和烈酒焦糖中存在的低分子量碳水化合物(当使用时)。苏格兰威士忌中的糖浓度通常<200 mg/L。发现12年陈酿的豪华调和苏格兰威士忌含有50 mg/L葡萄糖、50 mg/L果糖和20 mg/L蔗糖。测试样品可通过直接进样离子交换色谱结合脉冲安培检测或气相色谱(将样品干燥后,将糖分离为其三甲基甲硅烷基醚衍生物)进行分析。从橡木木材中提取的碳水化合物衍生的其他糖可能以低得多的相对浓度检测到。
挥发性酚类同系物
-
在用于麦芽大麦窑干的泥炭中使用的威士忌中发现了各种挥发性酚类化合物。这些风味同系物存在于许多苏格兰麦芽威士忌中,特别是来自艾莱岛的那些麦芽威士忌,艾莱岛是苏格兰西海岸有八家蒸馏厂的岛屿。此外,在许多用这种麦芽威士忌制成的调和苏格兰威士忌中也发现了挥发性酚类。
-
挥发性酚类同系物最好通过直接进样反相梯度洗脱HPLC结合荧光检测,在内标(如2,3,5-三甲基苯酚)存在下测定(Aylott等人,1994)。该分析检测苯酚、愈创木酚、甲酚和二甲酚的异构体、丁香酚和其他酚类衍生物(图14.4)。或者,许多这些化合物可以通过毛细管柱气相色谱分离,并使用2,4-二硝基苯基衍生物获得增强的灵敏度和选择性(Lehtonen,1983b)。
威士忌生产过程中的质量保证与分析
麦芽制造、发酵、蒸馏和陈酿
- 蒸馏厂需要具有特定属性的谷物,如低氮含量、已知水分含量和适当的麦芽制造特性。麦芽大麦品种可能需要进行真实性验证。通过实验室试验测试发酵效率可预测蒸馏厂的潜在产量,同时有一系列技术可用于蒸馏厂工艺故障排除(Hardy和Brown,1989)。此外,发酵、蒸馏和陈酿过程中的常规工艺分析通常仅限于感官评估和酒精度测量。
调配和装瓶
-
调配和装瓶过程中的主要分析(连同感官评估)是酒精度测量,现代设施采用电子密度测量。用于最终稀释至装瓶强度的水的质量非常重要。通常使用城镇供水,但通常会经过去矿化、活性炭和紫外线处理,以将痕量阴离子和阳离子降至最低,并消除任何异味风险。电导率测量用于监测水处理过程以及与pH测量相关的瓶装产品特性。
-
颜色一致性也是重要的质量参数,特别是对于那些添加微量烈酒焦糖以实现颜色标准化的威士忌。颜色通常通过在约500 nm波长的可见分光光度法进行监测,所得色度为选定固定波长下的吸光度×100。
-
威士忌通常通过粗滤和精滤片或滤芯过滤,以确保产品清澈明亮。有时会使用冷冻过滤,即液体在过滤前先冷却,以在长期寒冷环境储存条件下实现增强的稳定性。透明度或浊度使用浊度计测量,仪器由Sigrist-Photometer(瑞士恩内特布根)和Hach®(科罗拉多州拉夫兰)制造。
威士忌稳定性
-
在瓶中,威士忌是非常稳定的产品。只要瓶盖在玻璃瓶上密封良好,酒精度和主要挥发性同系物浓度将保持恒定,产品特性也不会改变(Aylott和MacKenzie,2010)。在温暖温度下储存会导致乙醛和乙酸乙酯浓度略有升高。如果瓶盖松动,乙酸乙酯和其次乙醛浓度会因挥发而降低,酒精度也会损失。在聚对苯二甲酸乙二醇酯(PET)5厘升瓶中对苏格兰威士忌进行两年的稳定性测试表明,由于水优先通过瓶壁迁移,酒精度略有上升。通过HPLC还检测到微量的对苯二甲酸乙二醇酯环状三聚体从PET迁移到烈酒中,浓度处于亚μg/L水平(Aylott和McLachlan,1986)。
-
过滤后的威士忌通常是清澈明亮的产品,但苏格兰威士忌偶尔会出现两种形式的絮凝。第一种形式称为“可逆絮凝”,当威士忌在极寒温度下长期储存时(如冬季运输中可能遇到的情况)会形成。威士忌会出现浑浊,当液体变暖并摇晃时浑浊消失。在“可逆絮凝”中检测到的主要同系物是长链脂肪酸的乙酯和较大的烷基酯,两者均可通过毛细管柱GC-MS检测。由于威士忌生产后要分销到全球各种气候条件下,发现通过在装瓶前对威士忌进行冷冻过滤可最大限度减少“可逆絮凝”的形成。该过程降低了形成“可逆絮凝”物质的浓度,且对产品特性无影响。
-
第二种絮凝称为“不可逆絮凝”,表现为草酸钙的微小晶体,当威士忌中天然低mg/L浓度的草酸与类似低浓度的钙离子反应时,会在威士忌中缓慢形成并沉淀。草酸可通过离子色谱法测定,钙可通过火焰原子吸收分光光度法测定。通过确保用于最终稀释的水去矿化以将钙浓度保持在最低水平,可消除“不可逆絮凝”的形成。田纳西威士忌的工艺包括在陈酿前让新蒸馏液渗滤枫木炭,也会从木材中吸收钙,可使用离子交换处理降低钙含量。
威士忌中的污染异味
-
瓶装产品中偶尔会报告有异味。较常见的异味问题源于威士忌在不合适的环境条件下运输和储存。例如,在靠近气味强烈的化学品处运输和储存会导致异味渗入瓶中。使用滚压防盗(ROPP)瓶盖的瓶子更能抵抗异味渗入。在下面描述的每个例子中,与GC-MS并行使用的GC-嗅闻法有助于识别有害污染物。
-
在许多情况下,从遥远市场退回的消费者投诉样品中检测到萘气味(樟脑丸味)的渗入,这些产品曾在不合适的环境条件下储存。萘在威士忌中的感官阈值非常低(产品中通常为μg/L水平),其存在可通过带荧光检测的HPLC或带选择离子监测的GC-MS进行定量。威士忌中也可能遇到霉味化合物。第一个例子是1,3,5-三氯苯甲醚(TCA),这是一种特别难闻的化合物,已被多次报道(Saxby,1996)。当优质瓶装产品储存在炎热、潮湿和潮湿的气候条件下(如南亚地区),会发现亚μg/L水平的TCA污染。据认为,用于制造纸箱和箱子的纸浆中的痕量三氯酚可经过微生物降解形成TCA,然后通过瓶盖/瓶子接口进入产品。第二个霉味例子是土臭素污染,由储存于潮湿条件下的谷物在发酵前的微生物活动引起。这种霉味/土腥味化合物的痕量μg/L浓度可通过发酵、蒸馏和陈酿过程带入,污染最终的威士忌。
消费者问题
-
分析在检查消费者退回的投诉样品时非常有用。考虑到全球销售的威士忌瓶数量巨大,消费者投诉的数量通常很少。这归因于威士忌的内在稳定性以及整个威士忌制造过程中应用的非常高的质量标准。
-
质量实验室收到消费者投诉时的首要要求是确认其有效性和可能的原因。现在大多数威士忌生产商在其瓶子上都有“追踪”标记,提供了其产品制造供应链的大量详细信息。这些标记称为“批号”,通常位于瓶颈附近、瓶底附近的侧面或标签后面的玻璃上。可以找到诸如批次号、装瓶日期、装瓶线号、发货日期和第一个客户身份等信息。此类信息在调查消费者和质量问题时非常有用。
-
有效的消费者投诉可分为两类:由包装问题引起的投诉和由液体问题引起的投诉。包装类投诉通常源于供应商问题、生产线质量问题或分销过程中造成的损坏。通过在制造过程的材料供应和验收中采用适当的标准和质量保证程序,可将包装线问题降至最低。现代玻璃瓶在玻璃制造过程的热端用氧化锡处理以 toughen 玻璃,在冷端用表面活性剂和油酸处理,使玻璃在处理过程中具有抗划伤性。偶尔,油酸的过度应用会导致产品中出现该酸的小油滴污染。
-
有时,消费者可能会无意中用使威士忌不稳定的物质污染其威士忌。例如,微量牛奶会导致不溶性牛奶和威士忌成分的大量沉淀。这种污染可通过检测上清液中的乳糖(来自牛奶)和沉淀物中的乳脂(用三氟化硼/甲醇衍生化后作为甲酯分析)来表征。
-
以类似的方式,低mg/L浓度的铁与陈酿同系物反应会导致绿色变色,当铁浓度达到10 mg/L时几乎变为黑色。蒸馏后过程中的铁锈可能非常有害,工艺工程师可通过在罐和管道构造中使用高级不锈钢来最大限度降低这种风险。
威士忌的真实性
- 威士忌真实性分为两类:品牌真实性和一般真实性。品牌真实性关乎消费者所购瓶中液体是否与标签上的品牌名称相符。一般威士忌真实性则适用于相关液体是否有资格被宽泛地描述为“威士忌”。在这两种情形下,液体分析都扮演着重要角色,它通过将可疑样品的分析指纹与正品品牌或威士忌类型的分析指纹进行比对来发挥作用。
品牌真实性
-
威士忌品牌真实性分析能让执法机构保护消费者,同时帮助生产商保护其品牌免受非法替换和伪造行为的侵害。替换行为发生在酒吧中时,通常是将一种品牌故意非法地替换为另一种更便宜的品牌。当这种情况出现,消费者、品牌所有者,甚至酒吧所有者往往都会被欺骗。消费者保护官员从酒吧收集可疑样品,并将其提交给他们的支持实验室或品牌所有者进行真实性分析。在英国,这项工作由地方当局的贸易标准部门或环境卫生部门负责,并有公共分析师提供支持。许多其他国家也有类似的资源,且通常会得到品牌所有者及其行业协会的支持。
-
在混合苏格兰威士忌的案例中,人们发现对主要挥发性同系物(尤其是高级醇)进行分析,能够设定正常的同系物浓度范围(Aylott,2010;Aylott 等人,1994)。例如,表14.2展示了三种不同品牌的混合苏格兰威士忌的正常分析范围数据。这三个品牌包含着截然不同的麦芽和谷物威士忌混合比例,从它们的2-甲基丁醇和3-甲基丁醇的浓度范围中便可看出。由于价格较低的品牌往往含有较低比例的麦芽威士忌,所以这些通常是被用于非法重新灌装更昂贵产品瓶子的那种产品类型。
表14.2 三种不同品牌苏格兰威士忌样品的主要挥发性同系物浓度范围(g/100 LAA),分别取自42、54和42个生产批次
| 样品 | 宣称酒精度(%) | 乙醛 | 甲醇 | 乙酸乙酯 | 正丙醇 | 异丁醇 | 2-甲基丁醇 | 3-甲基丁醇 | 2-和3-甲基丁醇 | 比率1 | 比率2 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 品牌A | 40 | 3.4–8.4 | 6.4–9.9 | 20–24 | 50–58 | 61–70 | 10–13.7 | 32–39 | 42–53 | 0.7–0.8 | 2.8–3.1 |
| 品牌B | 40 | 3.3–8.6 | 6.2–10 | 21–27 | 51–66 | 61–72 | 16–21 | 46–56 | 62–76 | 0.9–1.1 | 2.7–3.0 |
| 品牌C | 40 | 6.6–13 | 6.0–9.2 | 34–42 | 58–87 | 64–76 | 22–26 | 60–70 | 82–96 | 1.2–1.3 | 2.6–2.8 |
比率1 = 2-和3-甲基丁醇/异丁醇。
比率2 = 3-甲基丁醇/2-甲基丁醇。
- 对于可疑样品,分析人员会首先测定酒精度和主要挥发性同系物,然后将结果与正品品牌的正常范围进行比较。如果可疑样品的结果落在正常范围内,通常会认为该样品是真实的。如果结果超出正常范围,则样品不真实。表14.3还包含了三个可疑样品B1、B2和B3的结果,这些样品是消费者保护官员从酒吧收集的,装在标有品牌B的瓶子里出售。样品B1的结果落在品牌B的正常范围内,因此被认定为正品品牌B。样品B2的同系物浓度在该品牌的正常范围内,但酒精度为30% vol。结论是样品B2是正品品牌,但被掺假并通过加水稀释来扩大体积。样品B3的许多同系物超出了品牌B的正常范围(尤其是异戊醇),结论是它不是真正的品牌B,而是另一种混合苏格兰威士忌,其混合成分中的麦芽威士忌比品牌B少。这种分析方法经常为起诉那些在酒吧中将流行品牌替换为更便宜产品的人提供证据。
表14.3 苏格兰威士忌品牌真实性调查中的主要挥发性同系物浓度(g/100 LAA
| 可疑样品 | 酒精度(%) | 乙醛 | 甲醇 | 乙酸乙酯 | 正丙醇 | 异丁醇 | 2-甲基丁醇 | 3-甲基丁醇 | 2-和3-甲基丁醇 | 比率1 | 比率2 | 真实性 | 结论 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| B1 | 40.0 | 7.2 | 8.5 | 25 | 60 | 70 | 17 | 48 | 65 | 0.93 | 2.82 | 正品 | — |
| B2 | 30.2 | 5.0 | 6.0 | 22 | 55 | 70 | 20 | 54 | 68 | 0.97 | 2.7 | 非正品 | 加水稀释 |
| B3 | 40.0 | 9.0 | 5.0 | 15 | 39 | 75 | 13 | 35 | 48 | 0.64 | 2.7 | 非正品 | 其他苏格兰威士忌 |
| C1 | 40.1 | 11.7 | 8.8 | 32 | 70 | 73 | 22 | 62 | 84 | 1.15 | 2.8 | 正品 | — |
| C2 | 39.3 | 6.4 | 6.9 | 15 | 43 | 46 | 13 | 38 | 51 | 1.10 | 2.8 | 非正品 | 其他苏格兰威士忌 |
| C3 | 47.2 | 1.7 | 1.7 | 4 | 7 | 9 | 5 | 15 | 21 | 2.18 | 2.9 | 非正品 | 混合物 |
| C4 | 38.0 | 8.0 | 4.0 | 16 | 30 | 35 | 11 | 31 | 42 | 1.15 | 2.8 | 非正品 | 稀释 |
比率1 = 2-和3-甲基丁醇/异丁醇。
比率2 = 3-甲基丁醇/2-甲基丁醇。
一般真实性
-
一般真实性分析比品牌真实性分析更为复杂,因为所使用的分析数据必须涵盖该类别中的所有威士忌,而不是特定品牌较窄的分析指纹(艾洛特,2010;莱尔等人,1978;辛普金斯,1985)。一般真实性主要是监管较少市场的关注点,这些市场对威士忌的法律定义不太严格,消费者保护法律也不够严格。
-
色谱技术为可疑样品提供了定性和定量信息,以便与正品的已知分析范围进行比较。检查可疑产品中是否存在不属于一般威士忌的成分,或可疑产品中是否缺少必需的同系物,这也很有用。外来成分的存在或关键同系物的缺失将引发对一般真实性的怀疑。
-
主要挥发性同系物特征在一般真实性分析中非常有用。例如,异常高的甲醇浓度可能表明使用了非谷物酒精。存在3-甲基丁醇而没有任何2-甲基丁醇可能表明添加了3-甲基丁醇作为合成调味剂。成熟同系物特征也可以以类似的方式使用。成熟同系物的缺失可能表明可疑产品未经过所需的成熟期,而某个同系物(如香草醛)单独存在且没有相关的成熟同系物,可能表明其作为合成调味过程的一部分被添加。此类示例的分析结论可用于证明声称是威士忌的可疑产品未按照法规要求生产。分析证据可有助于取消可疑产品作为威士忌的资格。
-
最近,为谷物苏格兰威士忌、麦芽苏格兰威士忌和混合苏格兰威士忌建立了广泛的分析范围和同系物比率。当与上述知识结合时,就有可能开发出一种确定苏格兰威士忌一般真实性的实验方案(艾洛特和麦肯齐,2010)。由此产生的分析证据可帮助保护苏格兰威士忌的地理标志,并有助于取消虚假产品的资格。
-
同位素技术已被评估用于检查可疑样品中存在的酒精是否仅来自谷物发酵,而不是来自更便宜的碳水化合物来源,如甘蔗或甜菜。一种潜在的稳定同位素测量是乙醇中甲基和亚甲基氢的不同位置的²D/¹H比率,使用位点特异性天然同位素分馏-核磁共振(SNIF-NMR)确定。甲基氢主要受发酵底物的影响,而亚甲基氢受发酵水中比率的强烈影响(马丁等人,1995)。
-
¹³C/¹²C稳定同位素比率受可发酵底物用于同化CO2的光合作用途径的影响(帕克等人,1998)。大麦、小麦和甜菜使用C3(卡尔文)途径,而玉米和甘蔗主要使用C4(哈奇-斯莱克)途径。不幸的是,这种技术无法帮助验证许多由大麦和玉米制成的威士忌。最后,合成酒精显然不允许在威士忌中使用,通过液体闪烁计数进行的¹⁴C分析可用于区分烈酒和加强葡萄酒中的合成乙醇和天然乙醇(麦克韦尼和贝茨,1980)。
-
威士忌与所有酒精饮料一样,通常含有微量且无害的甲醇。造假者偶尔会通过用变性酒精或甲醇配制非法产品来制造健康危害。在这种情况下,分析人员可能需要解释异常高结果的意义(佩恩和戴恩,2001)。已开发出一种用于检测饮料中1%或更高甲醇的快速比色法(格雷厄姆等人,2012)。
真实性分析的新技术
-
为了创造验证威士忌品牌的新方法,各种研究人员考虑了气相色谱以外的多种技术。尽管通过气相色谱验证苏格兰威士忌品牌已被证明是可靠且广泛使用的,但它需要专业实验室,且分析过程可能相对昂贵和耗时。假冒调查受益于快速现场测试,因此开发了一种基于特定威士忌品牌紫外/可见光谱的筛选测试,可在几分钟内提供初步结果。使用存储在手持仪器内存中的参考数据,将可疑样品的光谱与正品品牌的光谱进行比较。现在可以快速筛选许多样品,只有可疑样品需要在实验室中进行确认性GC分析(麦肯齐和艾洛特,2004)。
-
以下总结了已测试用于威士忌验证的其他技术。热解-质谱,然后对所得质谱进行多变量分析,能够将非正品样品与正品品牌区分开来(艾洛特等人,1994)。痕量铜和其他金属分析被用作苏格兰威士忌真实性的指标(亚当等人,2002)。碳同位素比率被用于检测向苏格兰威士忌中非法添加中性酒精,为品牌和一般真实性分析提供了有用的技术(罗兹等人,2009)。在品牌真实性分析中展示了对烈酒和源水的²H和¹⁸O稳定同位素分析(迈耶-奥根斯坦等人,2012)。中红外光谱被用于检测假冒苏格兰威士忌(麦金太尔等人,2011),光流控芯片上的近红外光谱分析,然后进行主成分分析,被用于按酒厂、年龄和桶类型对麦芽苏格兰威士忌进行分类(阿肖克等人,2011)。纯美国威士忌通过糠醛与5-羟甲基-2-糠醛的比率进行验证(贾加那森和杜加尔,1999)。纯焦糖(E150a)是苏格兰威士忌中唯一允许的添加剂。液相色谱-质谱(LC-MS)被用于检测和区分威士忌中的焦糖E150a、b、c和d(库本等人,2012)。电喷雾电离质谱结合化学计量数据处理被用于检查来源和真实性(加西亚等人,2013;莫勒等人,2005)。
-
然而,需要建立分析策略来检查爱尔兰、加拿大和波旁威士忌品牌的品牌真实性。许多品牌,每个都有自己独特的混合成分,显示出重叠的分析指纹,使得上述苏格兰威士忌的色谱方法受到限制。
近期问题
亚硝胺
- 20世纪70年代末,在某些啤酒和威士忌中发现了低浓度(μg/L级)的N-亚硝基二甲胺(NDMA)。NDMA是一种疑似致癌物,因此需要分析方法来测定其浓度,并了解和控制其形成。NDMA化合物通过气相色谱分析,使用热能分析仪(TEA)作为检测器。这种分析对威士忌样品无需样品前处理,且灵敏度低于1 μg/L。当时对苏格兰威士忌的研究发现,NDMA的形成受麦芽大麦烘焙条件的影响。窑炉气体中氮氧化物(NOx)的存在会促进其形成。通过防止NOx进入系统或确保气流中存在二氧化硫,可以降低NDMA的水平(Duncan,1992)。使用重质燃料油而非天然气燃烧的麦芽窑中,二氧化硫水平会更高。如今NDMA问题已得到解决,苏格兰威士忌中已基本停止常规分析,仅对陈年样品偶尔进行分析。
氨基甲酸乙酯
-
20世纪80年代中期,在广泛的食品和酒精饮料中发现氨基甲酸乙酯(urethane)作为痕量成分存在。尽管氨基甲酸乙酯(EC)对实验动物是致癌物,但其浓度远高于酒精饮料中的含量,加拿大卫生福利部设定了餐酒(10 μg/L)、加强葡萄酒和清酒(100 μg/L)、蒸馏酒(150 μg/L)以及果酒、利口酒和葡萄白兰地(400 μg/L)的最大浓度(Connacher和Page,1986)。随后,欧洲和北美威士忌行业经历了为期五年的密集研究期,最初是为了以足够的灵敏度、选择性和精密度测定威士忌中EC的自然浓度,并了解其形成方式,以便实施控制措施(Zimmerli和Schlatter,1991)。各种调查显示,大多数混合苏格兰威士忌的EC浓度低于100 μg/L(Battaglia等人,1990;Dennis等人,1989;食品标准局,2000),尽管某些单一麦芽苏格兰威士忌中可能发现更高的浓度。同样,某些波旁威士忌超过了加拿大150 μg/L的限制。美国蒸馏商后来与酒精、烟草和火器管理局(BATF)达成一致,将新威士忌蒸馏液的EC目标限制设定为125 μg/L。最近,德国引入了400 μg/L的EC限制,因为某些果酒中EC水平较高。
-
测定威士忌和其他蒸馏酒中EC的方法需要毛细管柱气相色谱,结合氮特异性或质谱检测(Aylott等人,1987)。最初,EC通过溶剂萃取浓缩,但随后尽量减少样品前处理并实现方法自动化,采用直接注入威士忌样品并添加正丙基氨基甲酸酯作为内标。在极性毛细管柱上进行GC-MS,在m/z 62处进行质量检测,可实现良好的选择性,威士忌中的检测限<5 μg/L。发现分析蒸馏和陈酿强度样品时,EC的色谱峰形比40% vol酒精度的瓶装样品更好。因此,现在在进样前,先将瓶装强度样品用无水酒精(不含EC)稀释,使样品酒精度达到70% vol。
-
整个酒精饮料行业启动了深入研究,以了解EC的形成。当在苏格兰谷物威士忌工艺中发现由痕量氰化物和氰酸盐前体在蒸馏后形成EC时,威士忌研究取得了突破(Aylott等人,1990;MacKenzie等人,1990)。发现痕量氰化物来自蒸馏过程中发酵洗液中存在的异丁醛氰醇(IBAC)的热分解。IBAC在发酵过程中由酵母β-葡萄糖苷酶对天然存在的生氰糖苷表异树靛苷(EPH)的水解作用产生,该糖苷位于麦芽大麦的顶芽(生长芽)中(Cook等人,1990)。基于实验室的放射化学研究验证了这一化学途径(McGill和Morley,1990)。
-
科菲蒸馏器新制谷物烈酒中相对较低的EC水平可能因氰化物和氰酸盐前体在蒸馏后形成EC而增加,这一认识促使人们使用离子色谱结合电导和脉冲安培检测器研究其形成(MacKenzie等人,1990)。前体氰化物、氰化铜络合阴离子、乳腈和IBAC被共同测定为“可测量氰化物”(MC),以及氰酸盐和硫氰酸根离子。在新制烈酒中的MC浓度与所有可用MC前体在陈化前几周转化为EC后的最终EC浓度之间建立了实际关系(Aylott等人,1990),得出公式:
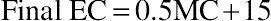
-
离子色谱或比色法MC分析被引入蒸馏过程控制。在这一研究期间,发现苏格兰谷物威士忌科菲蒸馏器中的牺牲铜表面以及向不锈钢美国波旁啤酒蒸馏器中添加牺牲铜环可吸附MC,从而帮助减少蒸馏后EC的形成。
-
更重要的是,发现不同大麦品种的EC前体水平不同(Cook,1990;Cook等人,1990)。首先,这一知识使麦芽制造商和蒸馏商能够选择低MC潜力的品种,种植者能够开发具有低表异树靛苷前体水平的新麦芽大麦品种。现在,所有威士忌中的氨基甲酸乙酯都可以通过蒸馏过程控制和使用低MC潜力的麦芽大麦品种进行监测,并将其形成降至最低。
消费者营养信息
-
与所有蒸馏酒一样,威士忌的标签遵循标准模式,包括产品品牌名称、类别名称(如苏格兰威士忌、纯波旁威士忌等)、酒精度、体积、生产者名称和地址,以及出口市场中的当地经销商信息。标签法规变得越来越复杂,因为某些市场要求健康警告、单位酒精标签、男女每日最大建议摄入量、孕期饮酒警告和回收信息。
-
尽管酒精饮料仍免于营养标签,但生产者应准备好回答消费者的问题。例如,威士忌的能量值来自其酒精成分,每100 mL为91 kJ/222 kCal;仅含微量碳水化合物,脂肪和蛋白质为零(食品标准局,2002)。在英国,一个酒精单位是10 mL(8 g)乙醇,因此70 cL瓶装威士忌中40% vol酒精度含有28个酒精单位。然而,在欧盟其他地区以及澳大利亚和新西兰,一个酒精单位是10 g乙醇。美国要求以美国 serving 体积引用营养成分,而其他国家则以公制 serving 体积和“每100 mL”为基础。
-
为了最大限度地减少跨市场所需的标签数量、降低成本并促进贸易,共同的标签标准显然是可取的。生产者必须检查当地标签法规。
过敏原标签问题
- 欧盟是最早为含麸质的谷物等食品成分引入过敏原标签法规的市场之一(2003/89/EC指令附件IIIa)。尽管行业、医生和乳糜泻支持组织普遍理解,由谷物制成的蒸馏酒不含过敏原物质,但必须证明这一点。由于小麦和大麦含有麸质,行业开展了一项研究计划,表明使用小麦和大麦作为原料的蒸馏物中不含过敏原物质,并将研究结果提交给欧盟委员会。这导致委员会修订了原始指令,给予用于制造蒸馏物的谷物(及其他)豁免过敏原标签(欧盟委员会指令2007/68/EC)。
参考文献
-
Adam T, Duthie E, Feldman J. 关于使用铜和其他金属作为苏格兰威士忌真实性指标的研究. 《酿造研究所杂志》. 2002;108:459–464.
-
Ashok PC, Praveen BB, Dholakia K. 光流控芯片上的单一麦芽苏格兰威士忌近红外光谱分析. 《光学快报》. 2011;19(23):22982–22992.
-
Aylott RI. 确保品牌完整性:烈酒行业的假冒问题. 《酿酒师与蒸馏师国际》. 2010;50–52:4月.
-
Aylott RI, MacKenzie WM. 确认苏格兰威士忌一般真实性的分析策略. 《酿造研究所杂志》. 2010;116:215–229.
-
Aylott RI, McLachlan I. 与饮用烈酒接触材料的评估. 载于: Campbell I 编. 《第三届阿维莫尔麦芽、酿造和蒸馏研讨会论文集》. 伦敦: 酿造研究所; 1986:425–429.
-
Aylott RI, McNeish AS, Walker DA. 使用氮特异性和质谱检测测定蒸馏酒中的氨基甲酸乙酯. 《酿造研究所杂志》. 1987;93:382–386.
-
Aylott RI, Cochrane GC, Leonard MJ, MacDonald LS, MacKenzie WM, McNeish AS, Walker DA. 谷物基烈酒中氨基甲酸乙酯的形成. 第1部分. 陈酿谷物威士忌中蒸馏后氨基甲酸乙酯的形成. 《酿造研究所杂志》. 1990;96:213–221.
-
Aylott RI, Clyne AH, Fox AH, Walker DA. 确认苏格兰威士忌真实性的分析策略. 《分析化学家》. 1994;119:1741–1746.
-
Battaglia R, Connacher HBS, Page BD. 酒精饮料和食品中的氨基甲酸乙酯(urethane): 综述. 《食品添加剂与污染物》. 1990;7:477–496.
-
Baxter MS, Walton A. 过去一个世纪大气中碳-14浓度的波动. 《伦敦皇家学会会刊A》. 1971;321:105–127.
-
Beveridge JL. 麦芽蒸馏厂风味研究. 载于: Campbell I, Priest FG 编. 《第三届阿维莫尔麦芽、酿造和蒸馏研讨会论文集》. 伦敦: 酿造研究所; 1990:449–452.
-
《联邦法规法典》., 1998a. 27 CFR, 第1章. 第5部分—计量手册. 子部分C—计量程序. 第5.22节—身份标准.
-
《联邦法规法典》., 1998b. 27 CFR, 第1章. 第30部分—计量手册. 子部分D—计量程序. 第30.31节—酒精度的测定.
-
欧盟议会和理事会2003年11月10日第2003/89/EC号指令,修订关于食品中存在的成分指示的第2000/13/EC号指令. 附件IIIa.
-
2007年11月27日第2007/68/EC号委员会指令,修订欧洲议会和理事会第2000/13/EC号指令的附件IIIa,涉及某些食品成分. 附件.
-
2000年12月19日第2870/2000号委员会条例,规定了酒精饮料分析的共同体参考方法,附件1, III.2, L333/36-L333/46.
-
欧洲议会和理事会2008年1月15日关于酒精饮料的定义、描述、展示、标签和地理标志保护的第110/2008号条例,废除理事会第1576/89号条例.
-
Connacher, H.B.S., Page, D.B., 1986. 酒精饮料中的氨基甲酸乙酯: 加拿大案例史. 载于: 《Euro Food Tox II会议论文集:食品中天然毒物跨学科会议》(毒理学研究所、瑞士联邦理工学院和苏黎世大学编), pp. 237–242. 技术研究所、瑞士联邦理工学院、苏黎世大学.
-
Cook R. 苏格兰威士忌中氨基甲酸乙酯的形成. 载于: Campbell I 编. 《第三届阿维莫尔麦芽、酿造和蒸馏研讨会论文集》. 伦敦: 酿造研究所; 1990:237–243.
-
Cook R, McCaig N, McMillan JMB, Lumsden WB. 谷物基烈酒中氨基甲酸乙酯的形成. 第3部分. 主要来源. 《酿造研究所杂志》. 1990;96:233–244.
-
Cubbon S, McMillan D, Owen C, Goddall I. 防伪: 使用LC-MS检测和区分威士忌中的焦糖E150a、b、c和d. 载于: Walker GM, Goodall I, Fotheringham F, Murray D 编. 《蒸馏酒IV:科学与可持续性》. 诺丁汉: 诺丁汉大学出版社; 2012:381–387.
-
Dennis MJ, Howarth N, Key PE, Pointer M, Massey RC. 某些发酵食品和酒精饮料中氨基甲酸乙酯水平的调查. 《食品添加剂与污染物》. 1989;6:383–389.
-
Duncan REB. 《Glenochil的历史》. 爱丁堡: 联合蒸馏器; 1992:p. 41.
-
Duncan REB, Philp JM. 苏格兰威士忌的分析方法. 《食品与农业科学杂志》. 1966;17:208–214.
-
EEC., 1989. 1989年5月29日EEC理事会第1576/89号条例,制定关于酒精饮料的定义、描述和展示的一般规则. 《欧洲共同体官方杂志》, L160, 1.
-
Fitzgerald G, James KJ, McNamara K, Stack MA. 使用固相微萃取结合气相色谱-质谱对威士忌进行表征. 《色谱A》. 2000;896:351–359.
-
《食品和药物条例》., 1993a. B.02.010-023节. 加拿大渥太华.
-
《食品和药物条例》., 1993b. B.02.020-021节. 加拿大渥太华.
-
食品标准局., 2000. 威士忌中氨基甲酸乙酯调查, 信息表2/00, 5月.
-
食品标准局., 2002. 《麦坎斯和威杜森食品成分》, 第6版摘要版, p. 347. 皇家化学学会, 剑桥.
-
Garcia JS, Vaz BG, Corilo YE, Ramires CF, Saraiva SA, Sanvido GB, Schmidt EM, Maia DRJ, Cosso RG, Zacca JJ, Eberlin MN. 电喷雾电离-傅里叶变换质谱分析威士忌. 《食品研究国际》. 2013;51:96–106.
-
Graham S, Holmes S, McGhee B, Tester R, Kariagin A, Steiner B, Sarver R. Alert® 甲醇检测, 一种快速诊断测定法,用于检测蒸馏酒中的甲醇污染. 载于: Walker GM, Goodall I, Fotheringham F, Murray D 编. 《蒸馏酒IV:科学与可持续性》. 诺丁汉: 诺丁汉大学出版社; 2012:209–212.
-
Hardy PJ, Brown JH. 过程控制. 载于: Piggott JR, Sharp R, Duncan REB 编. 《威士忌的科学与技术》. 哈洛: 朗曼科技; 1989:182.
-
HMSO., 1990. 《1990年苏格兰威士忌令》(法定文书: 1990), p. 1. 女王陛下文书局, 伦敦, p. 1.
-
Horwitz, W., 编., 2000. 《AOAC国际官方分析方法》, 第17版, 第II卷, 第26章, pp. 26.1.07-26.1.11. AOAC国际, 盖瑟斯堡, MD.
-
Jaganathan J, Dugar S. 通过测定糠醛与5-羟甲基-2-糠醛的比率验证纯威士忌. 《AOAC杂志》. 1999;82:997–1001.
-
Kahn JH. 威士忌、葡萄酒和啤酒中鉴定的化合物. 《AOAC杂志》. 1969;52(6):1166–1178.
-
Kelly J, Chapman S, Brereton P, Bertrand A, Guillou C, Wittkowski R. 气相色谱法测定酒精饮料中的挥发性同系物: 实验室间研究. 《AOAC杂志》. 1999;82:1375–1388.
-
Lee K-YM, Paterson A, Birkmyre L, Piggott JR. 不同产品类别的混合苏格兰威士忌顶空同系物的SPME分析. 《酿造研究所杂志》. 2001;107:315–332.
-
Lehtonen M. 气相-液相色谱法测定成熟蒸馏酒精饮料中的挥发性酚类. 《AOAC杂志》. 1983;66:62–70.
-
Lehtonen M. 高效液相色谱法测定成熟蒸馏酒精饮料中的非挥发性酚类化合物. 《AOAC杂志》. 1983;66:71–78.
-
Lisle DB, Richards CP, Wardleworth DF. 蒸馏酒精饮料的鉴定. 《酿造研究所杂志》. 1978;84:93–96.
-
Livermore D. 近红外反射(NIR)用作加拿大威士忌陈化的预测工具. 载于: Walker GM, Goodall I, Fotheringham F, Murray D 编. 《蒸馏酒IV:科学与可持续性》. 诺丁汉: 诺丁汉大学出版社; 2012:35–45.
-
Maarse, H., Visscher, C.A., 1985a. 《食品中的挥发性化合物: 定量数据》, 补编4, p. 66.1. TNO-CIVO食品分析研究所, 荷兰Zeist.
-
Maarse, H., Visscher, C.A., 1985b. 《食品中的挥发性化合物: 定性数据》, 补编2, p. 66.14. TNO-CIVO食品分析研究所, 荷兰Zeist.
-
MacKenzie WM, Aylott RI. 确认苏格兰威士忌真实性的分析策略. 第II部分. 移动品牌认证. 《分析化学家》. 2004;129:607–612.
-
MacKenzie WM, Clyne AH, MacDonald LS. 谷物基烈酒中氨基甲酸乙酯的形成. 第2部分. 苏格兰谷物威士忌中氨基甲酸乙酯形成所涉及的氰化物相关物质的鉴定和测定. 《酿造研究所杂志》. 1990;96:223–232.
-
Martin GE, Burgraff JM, Dyer RH, Buscemi PC. 酒精产品中同系物的气相-液相色谱测定及气相色谱/质谱确证. 《AOAC杂志》. 1981;64:186–193.
-
Martin GG, Symonds P, Lees M, Martin ML. 发酵饮料的真实性. 载于: Lea AGH, Piggott JR 编. 《发酵饮料生产》. 格拉斯哥: Blackie学术与专业出版社; 1995:386–412.
-
McGill DJ, Morley AS. 谷物基烈酒中氨基甲酸乙酯的形成. 第4部分. 放射化学研究. 《酿造研究所杂志》. 1990;96:245–246.
-
McIntyre AC, Bilyk ML, Nordon A, Colquhoun G, Littlejohn D. 使用包含多晶卤化银纤维的衰减全反射探针的中红外光谱法检测假冒苏格兰威士忌样品. 《分析化学学报》. 2011;690:228–233.
-
McWeeny DJ, Bates ML. 区分烈酒和加强葡萄酒中的合成乙醇和天然乙醇. 《食品技术杂志》. 1980;15:407–412.
-
Meier-Augenstein W, Kemp HF, Hardie SML. 通过²H和¹⁸O稳定同位素分析检测假冒苏格兰威士忌. 《食品化学》. 2012;133:1070–1074.
-
Møller JKS, Catherino RR, Erberlin MN. 威士忌的电喷雾电离质谱指纹图谱: 产地和真实性的直接证明. 《分析化学家》. 2005;130:890–897.
-
Paine AJ, Dayan AD. 定义酒精饮料中甲醇的可耐受浓度. 《人类与实验毒理学》. 2001;20:563–568.
-
Parker IG, Kelly SD, Sharman M, Dennis MJ, Howie D. 利用气相色谱-燃烧-同位素比质谱法研究苏格兰威士忌同系物的碳同位素比(¹³C/¹²C)以调查品牌真实性. 《食品化学》. 1998;63:423–428.
-
Philp JM. 陈化过程中苏格兰威士忌风味的发展. 载于: Campbell I, Priest FG 编. 《第二届阿维莫尔麦芽、酿造和蒸馏会议论文集》. 伦敦: 酿造研究所; 1986:148–163.
-
PRC., 2008. 中华人民共和国国家标准, GB/T11857—威士忌.
-
Reazin GH. 桶化学与威士忌陈化. 《酿酒师卫报》. 1979;108(6):31–34.
-
饮用烈酒分析研究委员会., 1979. 《饮用烈酒分析方法》. LGC, 米德尔塞克斯.
-
Rhodes CN, Heaton K, Goodall I, Brereton PA. 气相色谱碳同位素比质谱法应用于苏格兰威士忌中中性酒精的检测: 一种内部参考方法. 《食品化学》. 2009;114:697–701.
-
Saxby MJ, 编. 《食品污染与异味》. 格拉斯哥: Blackie学术与专业出版社; 1996.
-
《苏格兰威士忌法》, 1988, http://www.legislation.gov.uk/ukpga/1988/22/contents.
-
Shoeneman RL, Dyer RH. 苏格兰威士忌的分析概况. 《AOAC杂志》. 1973;56:1–10.
-
Simpkins WA. 非法烈酒检测中的同系物特征. 《食品与农业科学杂志》. 1985;36:367–376.
-
Singer DD, Styles JW. 饮用烈酒中高级醇的测定: 比色法和气相色谱法的比较. 《分析化学家》. 1965;19:290–296.
-
SWA. 《2009年苏格兰威士忌法规: 生产者和装瓶商指南》. 爱丁堡: 苏格兰威士忌协会; 2009.
-
Swan JS, Howie D, Burtles SM, Williams AA, Lewis MJ. 苏格兰威士忌风味的感官和仪器研究. 载于: Charalambous G, Inglett G 编. 《食品和饮料的质量》. 纽约: 学术出版社; 1981:201–223.
-
Zimmerli B, Schlatter J. 氨基甲酸乙酯: 分析方法、存在、形成、生物活性和风险评估. 《突变研究》. 1991;259:325–350.
下一章:第15章:副产品
回到目录