《威士忌生产工艺与营销策略(第二版)》第六章
第 6 章:苏格兰威士忌 —— 原料选择与加工
Tom A. Bringhurst
James Brosnan
摘要
苏格兰麦芽威士忌与谷物威士忌的生产已发生诸多变革,既要满足不断扩大的市场需求,又要符合可持续性与环境要求 —— 包括支持谷物供应链、降低能源与水的投入,同时将生产过程的环境影响降至最低。本章综述了麦芽威士忌与谷物威士忌的谷物原料选择及采购流程,并阐述了蒸馏厂当前采用的原料加工技术,涵盖麦芽蒸馏厂的糖化工艺、谷物蒸馏厂的蒸煮与转化技术,以及这些技术如何在现代可持续发展目标下演进。
关键词
大麦 育种 谷物 污染物 谷物(原料) 过滤槽 玉米 麦芽 泥煤处理 单一麦芽 软冬小麦 供应链 可持续性
引言
苏格兰威士忌的生产长期以来一直是大量出版物的主题,既有面向消费者的通俗指南,也有面向蒸馏行业从业者的技术论述。最新版《酒精教科书》(Ingledew 等,2009;Jacques 等,2003)为酒精生产的各个方面提供了有用的背景知识。Hume 和 Moss(2000)对麦芽威士忌和谷物威士忌的生产进行了简明且图文并茂的历史阐述。关于麦芽威士忌生产的技术细节可在 Piggott 等(1989)、Bathgate(1989, 1998, 2003)和 Dolan(2003)的著作中找到。Buglass(2011)总结了包括麦芽威士忌和谷物威士忌在内的多种饮用烈酒的生产。此外,还有一些关于谷物蒸馏的翔实论述,如 Pyke(1965)、Rankin(1977)、Bathgate(1989)、Wilkin(1989)、Piggott 和 Conner(1995)、Bringhurst 等(2003)、Collicut(2009)以及 Kelsall 和 Piggott(2009)的研究。
尽管部分早期文献年代已久,但仍包含相关信息。Briggs 等(2004)虽侧重于酿造,却对原料加工的主要阶段进行了详细阐述,这是深入理解谷物接收、研磨、糖化等技术的重要参考,且可应用于麦芽和谷物蒸馏。近年来,世界蒸馏酒会议的会议记录(Bryce 和 Stewart,2004;Bryce 等,2008;Walker 和 Hughes,2010;Walker 等,2012)是了解苏格兰威士忌及其他全球重要蒸馏酒产品最新发展的重要背景资料来源。Kelsall 和 Piggott(2009)提供了关于谷物、淀粉、研磨和一系列蒸煮工艺(包括低温和无蒸煮系统)的相对最新信息,这些内容也与苏格兰威士忌生产相关。
近年来,行业的显著变化正影响着蒸馏厂为满足当前及预期未来对苏格兰威士忌的需求而采用的技术。因此,现在是回顾苏格兰麦芽威士忌和谷物威士忌生产中谷物加工环节的适当时机。
在过去十年中,苏格兰威士忌蒸馏厂响应全球对其产品需求的扩张,不断增加谷物和麦芽烈酒的产量。部分通过以下方式实现:提升现有蒸馏厂的产能,通过提高原始比重、增加糖化桶装载量、增大洗酒量、缩短发酵时间等方式扩大现有工厂的利用率,以及对现有工厂进行现代化改造或安装新设备。一些公司目前正投资增加蒸馏厂产量, either 通过建造新蒸馏厂或大幅扩建现有设施。行业的持续成功还促使个体创业者、小型公司和大型组织重振衰落的蒸馏厂,并重新开放一些已关闭或封存的蒸馏厂。
因此,目前蒸馏厂工艺呈现出广泛的多样性,从生产能力约 5 万升纯酒精(LPA)的小型传统作坊式运营,到生产能力超过 1 亿升纯酒精的大型复杂现代化先进工艺(Gray,2012)。它们的共同之处在于均根据苏格兰威士忌的法律定义(European Parliament,2008;Statutory Instrument 2009,2009)生产烈酒,该定义规定必须在苏格兰使用水和谷物生产,加工成糖化醪,且仅通过内源性(麦芽)酶转化为可发酵底物,并由酵母发酵。不允许添加外部酶或其他工艺助剂(除了食用焦糖)。这一要求限制了苏格兰威士忌蒸馏厂的工艺选择,但对维持苏格兰威士忌生产的传统方面至关重要。
在苏格兰,两类威士忌蒸馏厂生产麦芽或谷物烈酒。当蒸馏厂生产新酒时,需至少陈酿 3 年,但通常陈酿 8 年或更长时间,然后才能作为单一麦芽威士忌或(很少见的)单一谷物威士忌装瓶。通常,成熟的麦芽和谷物烈酒混合在一起,生产出种类繁多的混合苏格兰威士忌品牌,这些品牌是该行业的主要产品。在全球范围内,苏格兰威士忌市场正在发生变化,尽管混合威士忌仍然非常重要,但对麦芽威士忌的需求大幅增长,因为消费者对这些极具个性的优质产品的品质认知日益提高。
可持续性日益成为谷物和麦芽蒸馏厂的主要考虑因素。其主要驱动因素包括:确保适合传统生产方法的原材料供应,以及确保该行业具有高知名度的全球品牌产品继续与纯净环境相关联(Hesketh-Laird 等,2012)。因此,蒸馏公司的重大投资必须考虑其对长期可持续性的影响,不仅是对单个公司,还包括对整个行业及其支持的各种供应链的影响,以及对环境的影响。这包括减少行业的整体环境影响,适应气候变化,并采取积极措施减少碳足迹。
在撰写本文时,苏格兰约有 100 家麦芽蒸馏厂在生产,每家都生产具有独特特征的麦芽烈酒。这不仅是单个蒸馏厂的基本属性,也是其预定混合产品的重要组成部分。一个高端品牌的混合威士忌可能包含多达 50 种不同的麦芽威士忌,以及作为混合基本基质的谷物威士忌。所有这些威士忌的年份都必须至少与标签上标明的一样。与麦芽威士忌相比,谷物威士忌的风味特征相对中性,这是由于使用连续分馏(或科菲)蒸馏器收集非常纯净和干净的烈酒的结果。然而,苏格兰威士忌谷物烈酒并非完全没有风味或香气,这对原材料和加工选择具有重要意义。
谷物威士忌的生产规模远大于麦芽蒸馏厂。谷物蒸馏厂的生产能力从 2500 万升纯酒精到 1.05 亿升纯酒精不等,平均为 5500 万升纯酒精。典型麦芽蒸馏厂的平均产能约为 300 万升纯酒精。2012 年,7 家运营中的谷物蒸馏厂生产的酒精(3.5 亿升纯酒精)超过了所有麦芽蒸馏厂的总产量(2.57 亿升纯酒精)(Gray,2012)。这强调了两种类型烈酒的生产相辅相成,都是苏格兰威士忌生产的重要方面。
本章重点关注苏格兰威士忌生产中麦芽和谷物蒸馏的原材料和加工方面,旨在提供蒸馏厂生产主要特征的简明易懂的概述。麦芽和谷物蒸馏厂有一些共同特征。它们都涉及谷物加工(麦芽蒸馏使用大麦芽,谷物蒸馏使用大麦芽和未发芽谷物的混合物)。它们使用研磨、蒸煮 / 糖化、发酵和蒸馏工艺的组合,根据苏格兰威士忌的官方法律定义生产饮用烈酒。然而,麦芽和谷物蒸馏厂在技术和蒸馏厂生产规模方面有几个重要区别。
一般来说,尽管单个麦芽威士忌蒸馏厂数量众多,但基本生产工艺实际上是相同的,只是在相对较小的细节上有所不同。相比之下,尽管谷物蒸馏厂数量较少,但它们能够使用更广泛的技术和工艺选择(在苏格兰威士忌定义的范围内),因此其生产技术的多样性要大得多。
本章的目的不是详细描述每个单独的工艺,而是参考所使用技术的各个方面来解释蒸馏厂加工的基本原理。然而,在仔细研究工艺本身之前,我们必须考虑麦芽和谷物蒸馏厂使用的主要原材料,并总结将谷物淀粉转化为可发酵糖(继而由酵母转化为酒精)的基本生物化学原理。
供应链可持续性
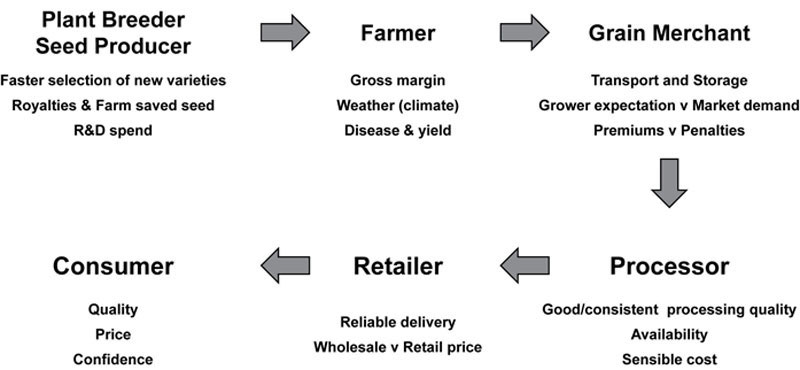
Brosnan 等人(2010)强调了支持谷物供应链可持续性的重要性,着重指出可持续性背后不同的经济、环境和社会因素。供应链的每个组成部分都有影响供应、价格和质量的不同视角与优先级,必须实现谨慎平衡才能使整个链条可持续。这一进程的关键驱动力来自植物育种者,他们的任务是开发能支持所有利益相关者的新谷物品种,并为创新和可持续性提供真正的技术路径(Brosnan 等,2010)。
可持续性现已成为苏格兰威士忌蒸馏厂的主要目标,该行业依赖确保优质谷物供应的连续性来维持和支撑其产品的发展与增长。供应链中的利益相关者紧密合作至关重要,以便种植者和谷物商人能清晰了解行业的战略需求(Brosnan 等,2010;Rae,2008)。
图 6.1 突出显示了将蒸馏用小麦生产作为可持续发展模型,其中可持续性、环境、经济和社会发展的主要互锁组件都对小麦供应链产生重大影响。Brosnan 等人(2010)确定了三个主要关注领域:(1)蒸馏厂需要易于获取的原材料;(2)他们更倾向于以合理价格购买谷物,避免市场波动的不确定性;(3)原材料必须在蒸馏厂中表现稳定。因此,为实现可持续性,必须将这些需求与其他供应链利益相关者的互补需求相平衡。其中一个重要特点是苏格兰威士忌蒸馏行业通过英国植物育种者协会,以及与英国农学领域的联系,以单个公司和行业的身份,成功努力发展并维持与植物育种者的联系。这体现在农业与园艺发展委员会(AHDB)等机构中,其中本土谷物管理局(HGCA)是重要组成部分,还有英国麦芽制造商协会(MAGB),每个机构都对新谷物品种的决策有重大投入。通过这些联系,蒸馏厂能够影响适合蒸馏的新小麦和大麦品种的开发与选择,同时也能为种植者、贸易商和其他供应链利益相关者带来良好回报。
原材料
苏格兰威士忌生产商使用的主要谷物原料为小麦和大麦。麦芽蒸馏厂使用大麦芽,而谷物蒸馏厂则使用小麦和玉米等未发芽谷物。多年来,尽管少数蒸馏厂仍在使用玉米,但其重要性已大幅下降,蒸馏厂已对工艺所需的大麦和小麦类型形成明确偏好。
就大麦而言,蒸馏厂寻求可由麦芽制造商制成麦芽的现代品种,以实现高酒精得率且易于加工。目前,这意味着他们需要低氮春大麦品种,其制成的麦芽应具有高可发酵浸出物含量,且麦芽改性程度足够,以赋予蒸馏厂良好的加工特性。
谷物蒸馏厂需要低氮软质冬小麦品种,这些品种需易于加工并能实现良好的酒精得率。它们通常归类为饲料小麦和饼干小麦,与优质面包用小麦的品质范围截然相反 —— 后者被认为不适合谷物蒸馏生产。由于饲料小麦的市场属性,蒸馏厂传统上以商品形式交易小麦,通常不会为这种基础原料支付额外溢价。蒸馏厂参与英国全国新小麦品种的筛选过程,促使更多适合谷物蒸馏的冬小麦品种得以推广。
新兴生物燃料行业的兴起最终将影响蒸馏用小麦的供应(及价格);随着该行业投产,可能会竞争英国可用蒸馏小麦的很大比例(每个生物乙醇精炼厂每年约 200 万吨)。
为确保谷物原料的可持续供应,苏格兰威士忌行业密切参与英国小麦和大麦的筛选过程,蒸馏厂与整个供应链保持联系。与植物育种者、种植者、农学家、麦芽制造商和其他终端用户等利益相关者的讨论至关重要,以确保有足够供应的适合蒸馏品质的大麦和小麦,同时兼顾其他终端用户的不同(有时是对立的)需求。
蒸馏厂与植物育种者之间的沟通,对于提供更适合其工艺的新大麦和小麦品种(以提高酒精产量和加工性能)至关重要。随着蒸馏厂对这些品质的理解加深,他们持续推动新蒸馏品种的开发。近年来,我们对重要品质性状遗传基础的认知扩展,使植物育种者能够更精准地识别合适的亲本品种,从而更高效地培育新的大麦(可能还有小麦)品种。这些品种不仅能为蒸馏厂带来显著优势,还能为整个谷物供应链提供更好的支持。
谷物育种
19 世纪,格雷戈尔・孟德尔(Gregor Mendel)确立了植物遗传学的基本原理。他发现了遗传性状 —— 这些性状会从亲代传递至子代。植物育种者的目标是重组这些被称为 “基因” 的遗传单位,以培育出具有改良特性的作物。实际上,这是一个复杂、耗时且昂贵的过程,因为每株植物包含数千个基因,育种者需要将一系列理想性状组合到同一植株中,才能培育出成功的新品种。
传统育种涉及选择特定的亲本植株(基因型),所选亲本通常具有高产农艺性状或抗病性等理想特征。育种者的技能在于从众多不同的子代中筛选出最优植株,这些植株会在试验田中种植并经过多年测试。典型流程包括检测大量单株植物的不同特征(表型性状),从农艺表现到终端用途品质均需评估。目前估计,育种者需种植和评估多达 100 万株单株植物,才能培育出一个商业上成功的小麦(或大麦)品种,而这一过程可能需要长达 15 年才能将产品推向市场(Brosnan 等,2010)。
现代(非转基因)遗传学的最新进展已识别出一些与小麦和大麦终端用户重要表型性状相关的基因,植物育种者正积极利用这些信息,通过经典非转基因育种技术加速育种进程(Sylvester-Bradley 等,2010)。现代研究的目标之一是开发需氮量和农艺处理更少的新品种,从而降低种植的经济和农艺成本,支持更适合英国市场的谷物品种,并为谷物供应链的长期可持续性提供支撑(Sylvester-Bradley 等,2010)。这些举措正促使大量优质大麦和小麦新品种涌现,它们不仅对麦芽和谷物蒸馏厂具有巨大应用潜力(Bringhurst 等,2012a),还因其更优的农艺性状和抗病性对种植者颇具吸引力。这些发展为蒸馏行业和整个谷物供应链的可持续性做出了积极贡献,并将推动植物育种者持续改良现代大麦和小麦品种。
大麦(及小麦)的选育无论形式如何,通常被认为起源于人类历史早期,至少可追溯至 1 万年前(Badr 等,2000)。如今在英国和欧洲种植的现代两棱大麦品种,是从适应北欧寒冷湿润气候的早期半野生地方品种逐步演化而来。这些原生地方品种为现代大麦育种者提供了丰富的遗传多样性,可用于开发新品种。这些地方品种的后代仍可被发现,少量古卓大麦(bere barley)至今偶尔用于小型麦芽蒸馏厂的生产。
麦芽蒸馏的原材料
大麦选择
现代麦芽大麦品种的选育已形成成熟体系。商业植物育种公司采用经典杂交技术每年培育新品种,新品种的筛选和测试耗时且昂贵,每个新品种需长达 15 年开发周期。开发时间包括育种者的初步筛选测试(9-11 年),随后在英国进行数年的国家列名(NL)试验。每个进入英国评估体系的新品种,育种者需投入约 100 万英镑。
某些大麦品种中含有的表异赤杨苷(EPH)是一种糖苷腈(GN),是氨基甲酸乙酯的主要前体物质(Cook, 1990)。苏格兰威士忌生产中培育新品种的难点之一是需选择不产生 GN 的品种。但并非所有大麦品种都产生 EPH,育种者可通过成熟的遗传标记筛选不含该前体的品种(Swanston 等,1999)。行业政策要求所有面向蒸馏市场的新品种均需鉴定为非 GN 产生型。针对其他重要终端用途性状的遗传标记已开发,但应用仍处于早期阶段。
新品种进入市场前,必须通过 “特异性、一致性和稳定性(DUS)” 测试,随后列入 HGCA 国家清单,这是所有进入英国种植市场的商业大麦新品种的强制要求。这确保品种具有独特属性,并在其生命周期内保持稳定,同时帮助确定新品种的目标市场(酿造、蒸馏或饲料)。
初始两年测试(NL1 和 NL2)目前由本土谷物管理局(HGCA)管理,旨在评估新品种是否适合英国种植、是否比现有品种具有农艺优势,以及是否易受病虫害影响。HGCA 大麦委员会每年审议试验数据,决定品种是否进入推荐清单(RL)试验阶段(通常再持续两年)。这些试验主要评估新大麦(和小麦)品种在英国商业种植的适应性,成功品种将列入年度 HGCA 推荐清单。
大麦采购与麦芽制作
苏格兰蒸馏厂目前每年使用约 70 万吨大麦芽,主要用于麦芽蒸馏,其中约 10% 用于高酶谷物蒸馏麦芽。蒸馏厂通常通过合同从商业麦芽商获取大麦芽供应,双方保持密切沟通以确保供应和终端需求匹配。在英国,多数大麦芽通过质量保证计划交易,如 MAGB 运营的 “英国保证标准”(MAGB, 2008),该计划支持食品安全、产品合法性、良好操作规范和产品质量,确保可追溯的大麦来源无霉菌毒素、农药残留、重金属等潜在食品安全问题。
尽管部分麦芽蒸馏厂仍保留少量地板制麦产能,但仅存的地板制麦多为小型设施,供应蒸馏厂总体麦芽需求的一小部分。其原料主要基于本地大麦,也可通过谷物贸易商或制麦公司从其他来源获取。地板制麦留存的主要原因之一是维持与行业传统的联系,同时为蒸馏厂产能提供补充,并赋予烈酒更独特的特征(如艾雷岛、奥克尼岛和其他岛屿威士忌)。
麦芽蒸馏厂通常需要低氮春大麦,易于制成高质量蒸馏麦芽,并具有高酒精得率和良好加工特性。典型蒸馏用麦芽大麦总氮含量为 1.40-1.60%(干基),氮含量与淀粉含量成反比,低氮大麦淀粉更多,酒精得率潜力更高。谷物蒸馏用大麦氮含量略高,接近 1.80-1.85%,以提供更高酶和氨基酸(游离氨基酸氮,FAN)生成潜力,这对谷物蒸馏厂至关重要。
泥煤处理
苏格兰威士忌生产中,地板制麦在麦芽烘烤过程中可赋予麦芽更特定的泥煤或酚类风味,这是某些烈酒的基本品质。其独特性源于当地开采的泥炭特征(Harrison 等,2006)。尽管商业麦芽商也可供应泥煤麦芽,但通常更通用,不一定反映单个蒸馏厂所需的特定特征。例外情况如艾雷岛,当地商业制麦设施靠近既定泥炭来源。
燃烧泥炭是传统方法,在烘烤过程中为大麦芽赋予泥煤、酚类、烟熏、焦香或药草特征。泥炭开采地点对泥煤麦芽的风味特征至关重要,进而影响烈酒的独特性。泥炭是 “在涝渍条件下由苔藓和其他苔藓植物、草本植物、灌木或树木部分分解形成的有机沉积物”(Harrison 等,2006)。在苏格兰,泥炭常见于艾雷岛和奥克尼岛等湿地,也存在于托明图尔和圣弗格斯(阿伯丁附近)等大陆地区。
麦芽规格
麦芽规格由蒸馏厂和麦芽商单独商定,并因商业交易、供应和收获质量而变化。表 6.1 显示了基于多种来源的典型麦芽规格,引用数值为指导值,可能随季节或供应情况调整。参数主要分为四类:(1)生产效率;(2)加工性能;(3)烈酒品质;(4)产品保护 / 尽职调查,每类均提供关键信息以判断麦芽批次是否适用。
| 大麦品种参数 | 指导值 | 备注 |
|---|---|---|
| 水分(%) | 4.5–5.0 | >6% 会导致储存 / 研磨问题 |
| 可溶性浸出物(0.2 mm 细粉)(%) | >79(83 dwb) | 最佳可用 |
| 可溶性浸出物(0.7 mm 粗粉)(%) | >78(82 dwb) | 最佳可用 |
| 细粉 / 粗粉差异(%) | <1.0 | 适度改性 |
| 可发酵性(%) | 87–88 | 最佳可用 |
| 可发酵浸出物(%) | >68 | 非必报 |
| 预测酒精得率(PSY,升 / 吨) | >410(430 dwb) | 最佳可用 |
| 糖化力(DP,α-、β- 淀粉酶) | 65–75 | 谷物蒸馏用 150–200 |
| 糊精化单位(DU,α- 淀粉酶) | >45 | 谷物蒸馏用 > 50 |
| 总氮(% 干基) | <1.5–1.6 | 取决于季节供应 |
| 可溶性氮比率(SNR) | <40 | 可溶性氮 / 总氮 |
| 游离 α- 氨基氮(FAN,ppm) | 150–180 | 高比重工艺需要更多 FAN |
| friability(%) | >96 | 谷物充分改性 |
| 均匀性(%) | >98 | 胚乳均匀改性 |
| 酚类含量(ppm) | 0–50 | 取决于客户需求 |
| SO₂含量(ppm) | <15 | 燃料来源 / 泥煤水平 / NDMA 风险 |
| 亚硝胺含量(ppm) | <1 | — |
| 糖苷腈(GN,g / 吨) | <1.2 | 优选非 GN 产生型 |
| 非 GN 产生型(g / 吨) | ~0.5 | 典型背景水平 |
表 6.1 2012 年典型麦芽规格
注:数值随季节变化,仅供参考。
来源:改编自 Dolan, T.C.S. (2003)
亚硝胺与硫
现代麦芽厂使用间接烘烤,已很好控制由大麦大麦碱与燃烧产生的环境氮氧化物(NOx)反应生成的亚硝胺(如 N - 亚硝基二甲胺,NDMA)水平。但泥煤麦芽需在烘烤过程中直接使用泥炭烟,或作为窑炉气流的额外输入,因此仍需通过燃烧硫(通常为 briquettes 形式)产生二氧化硫(SO₂),添加到穿过干燥麦芽的气流中,防止麦芽中形成亚硝胺。不同麦芽厂的硫化程度不同,但应足以将亚硝胺形成降至最低。过高 SO₂产生的酸性会导致设备腐蚀。过去曾使用高达 20-25 ppm 的硫,近期高泥煤麦芽规格限制最高 15 ppm。由于高硫(>15 ppm)会通过降低糖化醪 pH 影响麦芽可发酵性,重泥煤硫化麦芽需在运往蒸馏厂前陈化数周恢复。部分情况下,未泥煤麦芽可经低硫处理(最高 5 ppm)以降低潜在 NDMA 背景水平。
糖苷腈与氨基甲酸乙酯
氨基甲酸乙酯(EC)是蒸馏酒中的痕量污染物,在多个重要国际市场受监管。其形成路径已充分记录,主要前体为表异赤杨苷(EPH),一种存在于某些大麦品种中的糖苷腈(GN)(Cook, 1990)。目前通过关注蒸馏厂工艺(如制麦、蒸馏、铜器放置),但主要通过选择不产生 EPH 的蒸馏大麦品种来控制该污染物。当非 GN 品种(GN < 0.5 mg / 吨麦芽)稀缺或难以获取时,蒸馏厂也可使用低 GN 产生品种(如 Optic,GN < 1.2 mg / 吨)。但苏格兰威士忌行业政策规定,所有进入蒸馏大麦试验的新品种必须为 EPH(或 GN)非产生型(详见第 14 章)。
其他污染物
蒸馏厂需对原料中的霉菌毒素、农药和重金属等谷物污染物进行尽职调查测试,实际常由专业分包实验室执行。为降低供应链风险,MAGB、HGCA 等谷物质量保证机构也会定期委托这些污染物的谷物调查。
谷物蒸馏的原材料
谷物蒸馏用大麦
尽管与玉米和小麦相比成本相对较低,但未发芽大麦很少用于谷物蒸馏厂,因为其高含量的胶体(如 β- 葡聚糖)会导致加工问题(Walker, 1986)。在谷物蒸馏厂中,大麦通常以麦芽形式使用,其主要功能是作为酶的来源,将未发芽谷物(如小麦或玉米)中的淀粉转化为可发酵糖。根据苏格兰威士忌的法律定义,糖化醪中的所有酶必须来自麦芽,不允许添加其他外部酶。
谷物蒸馏用大麦麦芽(常称为高糖化力或高 DP 麦芽)必须含有高水平的淀粉降解酶。大麦麦芽中的酶水平通常以糊精化单位(DU)定义,这实际上是 α- 淀粉酶和糖化力(DP)的度量,采用 Analytica-EBC 方法 4.12 和 4.13(欧洲酿酒协会,2010)的标准方法测定。
谷物蒸馏用大麦必须含有高水平的 β- 淀粉酶,并具备产生高水平 α- 淀粉酶、极限糊精酶和 α- 葡萄糖苷酶的潜力。DP 为 180-200 单位且 DU 超过 50 单位的大麦麦芽仍被视为谷物蒸馏麦芽的标准要求(Bathgate, 1989)。由于大麦麦芽是谷物蒸馏厂生产过程中的较昂贵成分,因此持续推动减少麦芽用量,许多情况下麦芽添加率已降至 10% 以下。这使得谷物蒸馏麦芽满足高酶规格比以往任何时候都更为重要。
与壶式蒸馏(麦芽蒸馏)麦芽相比,谷物蒸馏用大麦的类型和生产工艺存在差异。谷物蒸馏用大麦通常比壶式蒸馏大麦含有更高的氮含量(1.8-2.0% N)(Bathgate 和 Cook, 1989)。这是因为谷物蒸馏厂更关注开发尽可能高的酶潜力,而非淀粉含量(尽管淀粉对酒精得率也有小而重要的贡献)。在谷物蒸馏麦芽的生产中,大麦发芽期更长(通常 5-6 天),并采用更温和的烘烤工艺(50-60°C)以开发和保留酶活性,将未发芽谷物淀粉转化为可发酵糖,并提供足够氨基酸支持发酵。
小麦
小麦是全球最重要的谷物之一,年全球产量约 6.5 亿吨(FAOSTAT, 2012),为世界提供了大部分营养(Uthayakumaran 和 Wrigley, 2010)。小麦不仅对食品生产重要,还广泛用于动物饲料和众多工业应用。
小麦属于小麦属(Triticum),包含多种物种,其中仅有两种(Triticum aestivum和Triticum durum)进行大规模商业种植。T. aestivum(六倍体)是常见的面包小麦,广泛用于面包、蛋糕、糕点、饼干、布丁等,以及淀粉生产、生物降解塑料和乙醇生产等工业应用(Uthayakumaran 和 Wrigley, 2010)。T. durum(四倍体)主要用于意大利面生产。普通小麦按种皮红色素强度分为红麦或白麦;按籽粒粉碎抗性分为硬质或软质;按对温度和环境条件的适应性分为冬麦或春麦(Uthayakumaran 和 Wrigley, 2010)。
小麦的主要应用利用胚乳中的淀粉和蛋白质储备(Wan 等,2008)。小麦的独特之处在于其形成面筋的能力,使其非常适合用于面包生产的面粉。然而,面包用面粉需要高蛋白(面筋)含量的硬质小麦,这与苏格兰威士忌生产所需的低蛋白(面筋)、高淀粉软质小麦截然不同(Brosnan 等,1999)。总体而言,蒸馏用小麦品种的品质更接近饲料和饼干用类型。
冬小麦是英国产量最高的谷物,播种面积最大。在苏格兰,冬小麦于 9 月下旬至 11 月播种,次年 9 月收获。作物生长期间严格控制氮肥施用,因为接近收获时施用的氮肥会在籽粒中积累,导致最终氮含量增加(Taylor 和 Roscrow, 1990)—— 这对蒸馏用小麦不利,但对面包小麦有利。苏格兰的收获天气往往使小麦天然含氮量低(Brown, 1990),因此通常更适合威士忌生产。除作为谷物威士忌、伏特加和金酒等饮用烈酒的生产原料外,小麦也是当前生物乙醇工厂的重要原料。
| NABIM 组别 | 类型 | 主要应用 | 备注 |
|---|---|---|---|
| 1 | 硬质 | 面粉加工和烘焙 | 优质,具有一致的研磨和烘焙性能。满足特定重量(76 kg/hL)、蛋白质(13%)和高果糖氮(∼250)的特定质量要求。品种不可互换,取决于终端用户需求。 |
| 2 | 硬质 | 面粉加工和烘焙 | 可变的优质面包制作潜力。部分品种表现一致,但不如第 1 组。其他品种表现不一致或适用于专业面粉。蛋白质含量低于第 1 组。 |
| 3 | 软质 | 饼干、蛋糕、蒸馏 | 用于饼干、蛋糕和其他面粉的软质品种;也包括一些蒸馏品种。质量要求包括软质研磨特性、低蛋白质、良好的提取率和可延展但无弹性的面筋。 |
| 4s/4h | 软质 / 硬质 | 蒸馏(仅软质)、通用、饲料 | 主要作为饲料品种种植的非优质品种,但磨坊主可能用于一些通用面粉。蒸馏厂将使用某些软质品种(不使用硬质品种)。 |
表 6.3 英国和爱尔兰磨坊主协会(NABIM)对英国冬小麦的分类
小麦规格
总体而言,蒸馏厂需要廉价、易加工且能提供可接受酒精得率的软质冬小麦。广义上,蒸馏用小麦的要求与饲料小麦的规格相似,这与面包生产不同 —— 面包磨坊主需要高品质、高氮和高面筋含量、淀粉含量相对较低的硬质小麦,并愿意为此支付溢价。符合面包制作规格的小麦通常不适合谷物蒸馏厂,因为可能导致蒸馏厂出现粘性问题,降低工艺效率并可能导致酒精得率低。这意味着蒸馏厂对小麦的需求不与面包磨坊主竞争,蒸馏厂可瞄准 “剩余优质” 小麦(Brown, 1990),从而以更经济的商品价格购买合适的小麦。
苏格兰威士忌谷物蒸馏对小麦的一般要求已确立(Agu 等,2006, 2008b;Bringhurst 等,2003;Brosnan 等,1999),主要包括软质胚乳质地、高淀粉含量、低总氮(蛋白质)和高酒精得率。其他一些参数也被认为对定义蒸馏品质重要,包括水分、高比重、籽粒大小、硬度和筛下物。最重要的决定因素是酒精得率与蛋白质含量之间的强负相关关系。在大多数情况下,不指定品种,尽管一些蒸馏厂可能有偏好的品种列表。然而,农艺系统的发展使得苏格兰的种植者市场强烈反映了蒸馏厂的终端用户需求。
新蒸馏小麦品种的选择
多年来,小麦品种 Riband 一直是蒸馏小麦的市场领导者(Lea, 2001),但在撰写本文时,该品种已被 Alchemy、Viscount、Horatio 和(可能的)Leeds 等更现代的品种取代,这些品种通过英国小麦推荐程序脱颖而出。该程序旨在评估和识别在农艺性能和终端用户品质方面更适合英国市场的新小麦品种。
每年,本土谷物管理局(HGCA)与英国植物育种者协会、国家农业植物学研究所(NIAB)和苏格兰农村学院(SRUC)合作进行一系列试验,不仅为蒸馏厂,也为其他终端用户(包括面粉磨坊主、面包师、饼干制造商以及动物饲料用户)评估新小麦品种。植物育种者最初将面向英国市场的新小麦品种提交至国家水平(NL)试验,为期两年(NL1 和 NL2)。如果试验成功,命名的新品种通常在一年后进入完整推荐列表(RL)试验。小麦试验每年在英国各地的多个地点进行,这使新小麦品种能在各种环境中测试,增加了试验过程的稳健性,并有助于识别特定的区域或市场适应性。在推荐程序的最后阶段,某些品种将获得临时或全面批准,其他品种将被拒绝。新品种在完成至少三年试验后才会获得批准。
HGCA 小麦委员会利用 RL 试验的结果为各个终端用户群体选择最有前途的新小麦品种,并将其列入年度 HGCA 和 SRUC 推荐列表。影响列入推荐列表的最重要参数涉及农艺因素,如农艺产量、发芽损伤倾向(即哈格贝格降落数值,HFN)、抗病性和秸秆强度。然而,终端用户品质数据和对特定应用(研磨、饼干 / 蛋糕制作、蒸馏)的适用性在推荐过程中也发挥重要作用。行业通过苏格兰威士忌研究所提供的蒸馏性能数据(基于酒精得率和粘度)是识别适合蒸馏的新品种的重要因素。
谷物加工
在详细探讨这些工艺之前,了解谷物加工的基础生物化学原理及其在蒸馏厂原料加工中的应用至关重要。核心关注点包括淀粉的结构与组成、淀粉糊化与回生、淀粉降解酶及其作用机制,这些均直接影响谷物在加工过程中的处理方式,以及淀粉向可发酵糖的转化效率。
淀粉结构
将淀粉高效转化为乙醇是蒸馏厂效率的主要决定因素,因为谷物蒸馏的首要目标是从原料中生产尽可能多的酒精。原料成本是蒸馏厂运营总成本的主要组成部分(Nicol, 1990),因此最大化酒精得率对蒸馏师至关重要。为实现原料的最大潜力,蒸馏师必须深入理解谷物淀粉的结构与特性,以及将其加工为可发酵底物(进而转化为酒精)的工艺影响。
淀粉结构与功能的基本原理已被认知多年,本文不旨在全面综述这一广泛领域,因其已在 Whistler 等(1984)、Pomeranz(1988)和 MacGregor 与 Bhatty(1993)等基础文献中充分记载。Kelsall 与 Piggott(2009)也对蒸馏厂相关内容提供了简明概述。
本节旨在简要概述与苏格兰威士忌生产中谷物加工特性直接相关的淀粉特性。过去十年中,尤其在淀粉精细结构及将淀粉降解为可发酵糖的酶类分类认知方面取得了一些进展,但总体而言,已确立的原理仍然有效。Pérez 与 Bertoft(2010)对淀粉结构及其组分进行了较新的全面综述,Bathgate 与 Bringhurst(2011)则对苏格兰威士忌生产的相关方面进行了概述。
淀粉颗粒与分子结构
苏格兰谷物威士忌生产的主要淀粉来源为小麦和玉米,不同谷物的淀粉组成与结构差异对蒸馏厂的加工方式具有重要影响,涉及可发酵糖转化及谷物处理效率的最大化。
淀粉是植物中仅次于纤维素的最丰富碳水化合物,是葡萄糖的缩聚物,存在于植物所有主要器官中,作为储存碳水化合物的主要形式,为休眠期提供储备食物(Swinkels, 1985)。在小麦、大麦和玉米等谷物中,储备淀粉主要储存于淀粉质胚乳,嵌入蛋白质基质中。淀粉以颗粒形式(尺寸范围 2-200 µm)沉积,在胚乳细胞的造粉体中积累。小麦淀粉主要由两类淀粉颗粒组成:大型透镜状 A 型颗粒(20-35 µm)和小型球形 B 型颗粒(2-10 µm)。通常,小颗粒数量远多于大颗粒,但大颗粒虽仅占颗粒总数的 12-13%,却包含超过 90% 的总淀粉(Bathgate 与 Palmer, 1973;Shannon 与 Garwood, 1984)。
与小麦不同,玉米淀粉颗粒形状不规则且呈多面体,通常更小,平均直径达 15 µm(Lynn 等,1997)。文献报道玉米淀粉颗粒尺寸范围为 3-26 µm(Swinkels, 1985),但其颗粒尺寸分布单一(Cochrane, 2000),而非小麦的双峰分布。
直链淀粉与支链淀粉
淀粉本身由两种主要成分组成:直链淀粉是由 α-(1,4) 连接的葡萄糖单元长链构成的线性分子,通常占总淀粉的 15-37%;支链淀粉具有高度分支结构,由大量相对较短的 α-(1,4) 连接链与 α-(1,6) 连接的分支组成,构成淀粉的主体。直链淀粉主要被认为具有规则的左手螺旋结构,而支链淀粉则主要呈结晶形式(French, 1984;Lineback 与 Rasper, 1988)。淀粉的性质受直链淀粉和支链淀粉相对含量的影响(Fredriksson 等,1998)。
小麦中的直链淀粉分子量为 10⁵-10⁶ Da,链长约 2000 个葡萄糖单元(Barnes, 1989),含相对少量的 α-(1,6) 分支(每 1000 个葡萄糖单元约 2-4 条链;每个分子 2-8 个分支点)(Hoover, 1995),表现出线性聚合物的特征(Lineback 与 Rasper, 1988)。
另一方面,支链淀粉是天然聚合物中分子量最高的之一(可达约 10⁸ Da),约为直链淀粉的 1000 倍(Barnes, 1989)。其高度分支结构由大量相对较短的葡萄糖链(10-60 个单元,平均约 20-25 个单元)组成(Cochrane, 2000),但总链长可达 2×10⁷个葡萄糖单元。分支点约占总葡萄糖单元的 5%(Swinkels, 1985),每 20-25 个残基约有一个分支点(Hoover, 1995)。支链淀粉被认为是决定淀粉物理和化学性质的主要因素(Tester, 1997)。
淀粉糊化
淀粉颗粒沉积后呈部分结晶状态,且在水中基本不溶。为利用淀粉,需破坏颗粒结构使其吸水(Evers 与 Stevens, 1985)。Zobel(1984)将糊化定义为淀粉颗粒膨胀和水合的过程,使淀粉可溶解。通常通过将淀粉与水制成浆液并加热至淀粉开始融化来实现,最终形成包含直链淀粉和支链淀粉片段的悬浮液,随后可被淀粉分解酶作用,转化为可发酵糖(Palmer, 1986)。
糊化分多个阶段:最初,当干燥淀粉颗粒在低温(0-40°C)下与过量水接触时,发生有限的可逆膨胀(无定形相);随着加热,结晶淀粉开始失去完整性(融化相),与非结晶部分结合后发生不可逆膨胀和水合(French, 1984),伴随粘度显著增加,这归因于淀粉颗粒中直链淀粉的溶出。膨胀伴随着淀粉颗粒内部分子秩序的破坏,表现为双折射消失(Atwell 等,1988;MacGregor 与 Fincher, 1993),这是在偏振光下观察淀粉颗粒有序度或结晶度的指标(Cochrane, 2000)。膨胀程度主要归因于支链淀粉的作用(Fredriksson 等,1998)。
糊化温度与粘度变化
淀粉颗粒糊化导致直链淀粉螺旋区解离和展开,支链淀粉结晶结构破坏,使游离的支链淀粉侧链水合和膨胀(French, 1984),导致淀粉颗粒膨胀,首先允许线性直链淀粉从颗粒中扩散出来,最终导致颗粒结构完全破坏。
直链淀粉比例与糊化起始温度呈负相关(Fredriksson 等,1998),即直链淀粉相对含量增加时,糊化起始温度降低。图 6.2 直观展示了淀粉颗粒开始糊化时发生的物理变化:从左到右,随着温度升高,淀粉颗粒因膨胀和糊化破坏而结晶度降低。
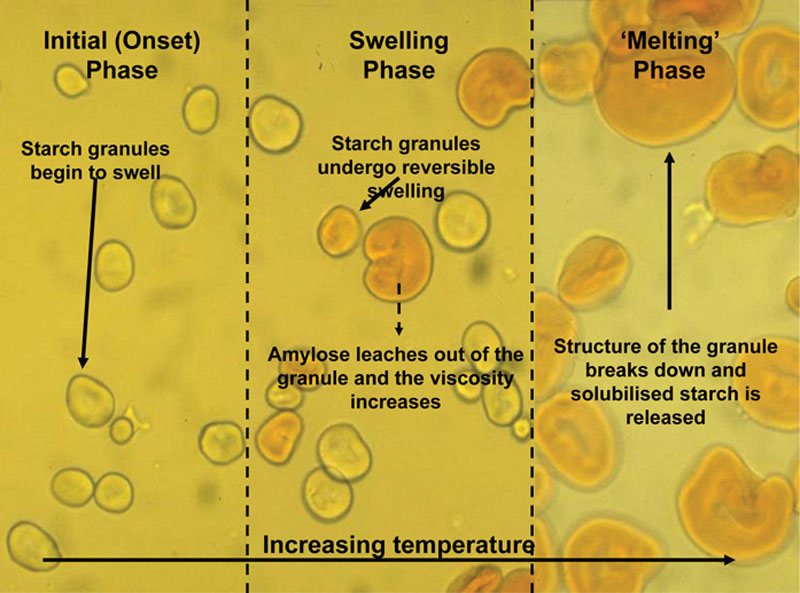
过去,测量谷物糊化温度的标准方法为差热分析(Zobel, 1984)或差示扫描量热法(Atwell 等,1988),但也通过其他技术研究糊化进程,如 Brabender 微粘度 - 淀粉图仪(Zobel, 1984),其在谷物浆液经历程序控温循环时测量粘度(糊化)变化。糊化被定义为糊化后颗粒膨胀和分子组分渗出(Atwell 等,1988)。微粘度 - 淀粉图仪的现代变体是由 Calibre Control 公司开发的快速粘度分析仪(RVA),图 6.3 展示了理想化的 RVA 淀粉糊化曲线,用于说明糊化过程的主要阶段。
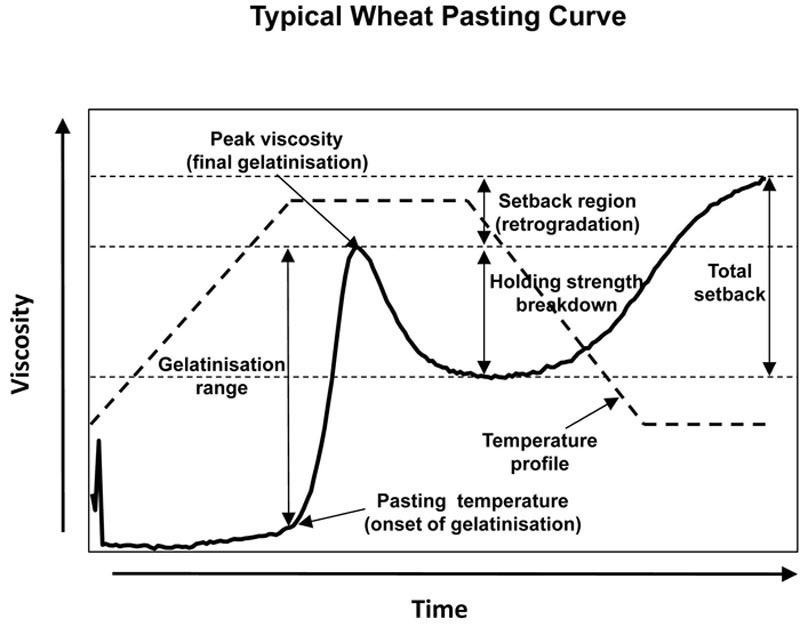
淀粉水解
由于未发芽谷物中的淀粉通常难以接触,需通过加热或蒸煮使其糊化以转化为可用形式。也可通过机械能量(如精细研磨或锤磨谷物)在较低温度下有效利用淀粉,这两种方式均有助于糖化醪中麦芽酶接触淀粉。
在麦芽蒸馏厂中,大麦芽中的酶(主要是 α- 和 β- 淀粉酶)可将淀粉和其他低聚糖转化为可发酵底物,发酵时被酵母转化为酒精。谷物蒸馏厂使用少量含高淀粉降解酶(统称为糖化力 DP,α- 和 β- 淀粉酶的混合物)和糊精化单位 DU(α- 淀粉酶)的大麦芽,将未发芽谷物淀粉转化为可发酵糖(包括葡萄糖、果糖、蔗糖、麦芽糖和麦芽三糖),以及线性和支链糊精与极限糊精(主要不可发酵)的混合物。
酶的作用机制
参与淀粉降解的主要酶是淀粉酶(Robyt, 1984),包括 α- 和 β- 淀粉酶,它们降解淀粉 α- 糖苷链中的 α-(1,4) 键。其中,α- 淀粉酶是最重要的淀粉降解酶,主要负责将淀粉降解为低分子量糊精和糖(Muller, 1991),其主要形式在 70°C 以下稳定,在钙离子存在下于 pH 6 发挥作用,但温度超过 67°C 时活性下降(Briggs 等,1981)。
第二种酶 β- 淀粉酶对将不可发酵糊精和低聚糖水解为可发酵糖(主要是麦芽糖,其次是麦芽三糖)至关重要。β- 淀粉酶的热稳定性低于 α- 淀粉酶,在正常糖化温度下会变性,65°C 下 40-60 分钟后活性完全消失(Briggs 等,1981)。67°C 会导致大量糊精残留,而非有效转化为麦芽糖(Palmer, 1989),这凸显了谷物和麦芽蒸馏厂生产中转化阶段精确控温的重要性。
蛋白质分解
转化的另一主要功能是蛋白质分解,通过该过程蛋白质被分解为氨基酸和其他低分子量含氮蛋白质片段(Boivin 与 Martel, 1991),为酵母提供可快速利用的必需营养源,使其在发酵过程中高效生长和作用。
蛋白水解酶(尤其是内肽酶)可能是糖化(转化)过程中理解最少的部分(Bamforth 与 Quain, 1989),但普遍认为麦汁中可溶性含氮物质的形成主要是热稳定内蛋白酶与热稳定羧肽酶协同作用的结果(Boivin 与 Martel, 1991;Briggs 等,1981),这些酶能够耐受糖化和转化过程中的温度(高达 65°C)(Bamforth 与 Quain, 1989)。
蛋白水解酶包括内酶(蛋白酶)和外酶(肽酶)的混合物。内蛋白酶(内肽酶)随机断裂多肽(蛋白质)的内部肽键,产生更小的分子,继而被羧肽酶(外酶)分解,从链的羧基端逐步去除氨基酸(Bamforth 与 Quain, 1989)。
然而,许多蛋白水解酶(如氨肽酶)以及一些内蛋白酶在 55°C 以上热不稳定,会被糖化过程中的条件灭活(Briggs 等,1981;Jones 与 Marinac, 2002),对麦汁的总可溶性氮含量贡献不大。因此,通常认为谷物蒸馏麦汁中的大部分游离氨基酸氮(FAN)源自麦芽蛋白水解,因为在正常蒸煮和转化条件下,蛋白水解酶失活,无法作用于未发芽谷物中的蛋白质。
麦芽蒸馏厂加工
麦芽蒸馏厂
麦芽蒸馏厂是苏格兰麦芽威士忌的基本生产单元。尽管所有麦芽蒸馏厂都具备主要基本特征,但其规模和技术可能存在显著差异。Bathgate(2003)强调了该工艺的传统性质,并指出麦芽蒸馏厂工艺的基础技术自19世纪以来几乎没有变化。当然,从那时起,工艺和设备都有了许多改进和优化,从而实现了更好的工艺控制和更高的效率。图6.5展示了典型苏格兰麦芽威士忌蒸馏厂的总体布局,突出了该工艺的主要特点。该工艺的主要输入是水、能源和大麦芽。在现代实践中,能源和水管理系统在某种程度上已集成到蒸馏厂工艺中。这些系统的范围可能从老旧小型蒸馏厂中非常小而基础的热和水回收系统,到大型现代化工厂中完全集成的能源和水管理系统。
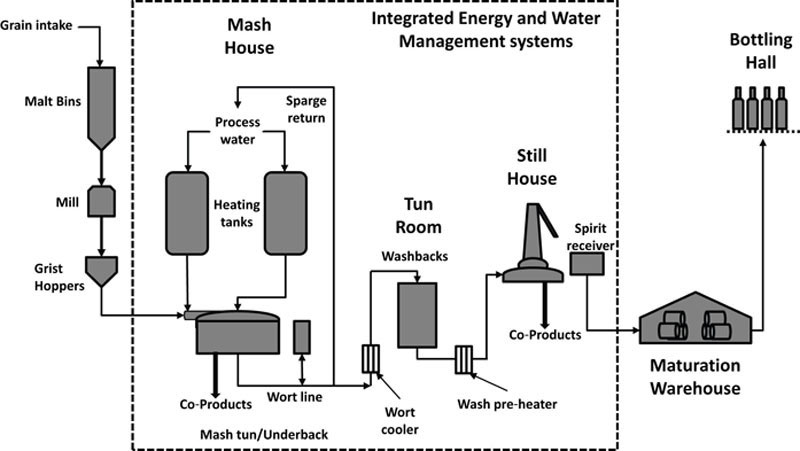
麦芽蒸馏厂工艺的主要部分包括谷物进料(谷物在此处交付、清洗并分配到麦芽仓,为生产过程做好准备)、研磨(将大麦芽粉碎成适合糖化工艺的麦芽粉)和糖化(将麦芽粉与热水混合,提取并过滤得到液体(麦汁),冷却后加入酵母,再添加到发酵罐(washbacks)中)。发酵后,酒液经蒸馏成为低度酒,然后再蒸馏成烈酒,如本出版物其他部分所述。蒸馏后,新制烈酒在橡木桶中于熟成仓库中陈酿至少3年,更典型的是8至12年,但对于优质麦芽威士忌,有时陈酿时间更长(超过20年)。陈酿后,成品威士忌被运至装瓶车间,在此将酒精度降至装瓶酒精度(通常为40%或43% abv),然后作为单一麦芽威士忌装瓶,或与其他麦芽威士忌混合成为混合麦芽威士忌,或与谷物威士忌和其他麦芽威士忌混合成为调和威士忌,之后投放国内或出口市场。
尽管每个麦芽蒸馏厂的工艺非常相似,但麦芽蒸馏厂的范围非常广泛。有些规模很小(50,000升/年),而有些则非常大(超过1000万升/年)(Gray,2012)。有些蒸馏厂具有非常传统的特点,如地板麦芽制造和传统糖化桶,而其他蒸馏厂则拥有更现代化的先进设备,如全过滤桶和高度集成的能量转移/回收系统。有些蒸馏厂古老而传统,保留了许多原始的工艺特点,从历史角度来看很有趣。这些特点促成了传统上与苏格兰威士忌相关的标志性形象,尽管此类单元的生产水平可能较低。一些更传统的蒸馏厂仍使用简单的锅炉房生产蒸汽,为蒸馏车间提供加热和动力所需的能源。
更现代化的蒸馏厂往往规模大得多,以反映行业现在所需的高生产水平。新建和较新的麦芽蒸馏厂还使用更先进的技术,现在通常设计(或改造)有现代化的能量回收和管理系统,这些系统与蒸馏厂工艺更充分地集成,使蒸馏厂能够通过从工艺的一个部分回收和转移热量(能量)到另一个部分来更高效地运行,同时减少用水量并限制向环境的排放。
大麦芽的加工
谷物进料
大多数大麦芽由商业麦芽制造公司(销售麦芽商)供应给麦芽蒸馏厂,并通过卡车(每车约20至30吨)运至蒸馏厂,在那里称重、目视检查并使用一系列简单快速的测试进行质量检测,然后通过麦芽进料系统(图6.6)通过传送带或谷物提升机卸料和输送。在进入麦芽仓之前,谷物会通过筛分系统去除灰尘、小谷粒和其他细小碎屑。该系统的一个重要部分是振动去石机,它将石头和其他重碎屑与谷粒分离。金属碎屑通常通过使谷物流通过强磁场来去除。如果不清除这些碎屑,当材料通过工艺时,极有可能损坏设备,并存在火灾或爆炸的严重风险。
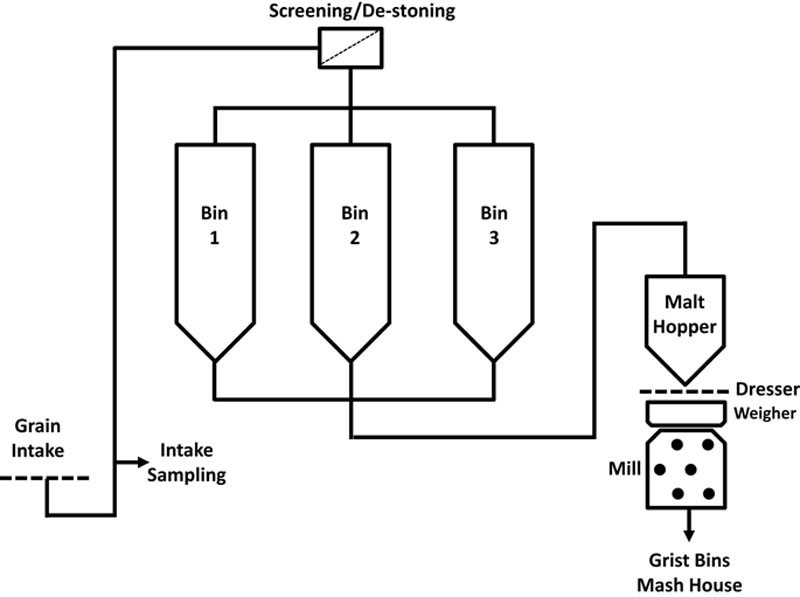
当大麦芽交付时,每车都会采样,要么使用采样探针手动采样,要么使用抓斗或自动滴流采样器机械采样。多个有代表性的样品会进行一系列质量检查。在接受交付之前,每批都会使用简单快速的测试进行分析,以确保其卫生、交付质量可接受且无异味。最重要的进料测试包括水分和氮(蛋白质)含量,通常使用近红外(NIR)分光光度法测量,以及千粒重和筛分(2.8毫米、2.5毫米、2.2毫米筛)。这些测试用于接受或拒绝该批货物。
如果可接受,该批货物将卸入谷物进料系统,并分配到下一个可用的麦芽仓。除非蒸馏厂想要隔离单个品种、质量等级或泥炭含量(取决于可用的存储容量),否则货物可能只是简单地添加到麦芽仓的现有内容中。根据可用性、质量和价格,蒸馏厂可能会收到单一品种的供应,或由麦芽商混合以满足特定质量规格的品种和麦芽批次的混合物。
在进料时,会采集额外的材料样品并送往实验室进行进一步分析,以确保材料符合所需的质量规格。通常,样品会在蒸馏厂保留一段指定的时间,以备将来出现质量纠纷时参考。如果与约定的规格有显著偏差,蒸馏厂可能会寻求赔偿。
麦芽加工
麦芽蒸馏厂的谷物加工可分为三个主要阶段:研磨、糖化/转化和麦汁分离。在研磨过程中,大麦芽被粉碎成麦芽粉,其成分适合在蒸馏厂工艺中加工。不同的蒸馏厂和糖化桶需要不同的麦芽粉成分。在糖化过程中,麦芽粉与热糖化液(洗糟水)混合,通常从先前的糖化中回收并转移到糖化桶(传统、半过滤或过滤桶)中,在标准糖化温度(63.5至64°C)下,麦芽中存在的淀粉降解酶将淀粉糊化并转化为可发酵糖。最后阶段是麦汁分离,在此过程中,甜麦汁从糖化桶中的谷物中过滤出来,然后泵送到发酵罐。然后,糖化桶中剩余的谷物用更高温度的第二和第三遍水提取——通常为70至75°C(第二遍水)和80至90°C(第三遍水和/或第四遍水)——以溶解剩余的淀粉和糖。第二遍麦汁通常用于填充发酵槽,而第三遍水则作为洗糟水返回加热罐用于下一次糖化。在糖化周期结束时,排出废谷物。这些废谷物用于动物饲料,并且通常在下次糖化之前用水清洗糖化桶。在现代实践中,在某些情况下,废谷物可能会进一步加工以提供可再生燃料——例如,通过使用厌氧消化系统。
由于糖化和发酵阶段不是在无菌条件下进行的,因此有效的清洁是蒸馏厂工艺的关键部分,因为它可以防止微生物感染的积累,否则可能导致潜在酒精产量的显著损失。通常每周一次或两次,使用苛性溶液或类似的清洁剂彻底清洁糖化桶和附属管道,并提起糖化桶板进行清洁。更现代的方法是使用独立的自动就地清洗(CIP)系统定期彻底清洁容器和管道。这些系统通常包括有效的喷雾系统,可以更彻底地覆盖否则通常难以接近的表面。这些可能包括用于清洁糖化桶板下表面的板下喷雾系统。(有关卫生的更多信息,请参见第17章。)
研磨原理
研磨是麦芽蒸馏厂工艺的关键部分,麦芽粉的组成在糖化过程中对麦汁分离的效率起着重要作用。尽管研磨后不应有完整的谷物残留,但最大限度减少对谷壳部分的损坏至关重要,因为谷壳是糖化桶中的主要过滤介质。完整的谷壳有助于通过减少麦汁流出时间来最大化提取效率。粗细颗粒的组成对提取效率和麦汁分离都很重要,因为高面粉含量会导致物质从糖化桶底部流失,从而可能损失提取物,而过多的细粉会堵塞糖化桶板并减少与废谷物的分离。因此,为每个蒸馏厂使用的特定糖化系统确定最佳或最实用的麦芽粉组成至关重要。Briggs等人(2004)强调,最佳研磨不易实现,有时在不同类型或批次的麦芽之间切换时需要调整磨机设置。
当蒸馏厂的麦芽供应发生显著变化或在不同批次的大麦芽之间切换时,定期检查麦芽粉组成非常重要。这可能需要对磨机设置进行一些调整,特别是当使用来自多个不同供应商的大麦时,其改性程度可能不同。与充分改性的麦芽相比,未充分改性的麦芽需要细磨,充分改性的麦芽容易破碎成更小的碎片。季节和环境变化以及不同品种的使用和可用性也是重要因素,因为这些会影响大麦的制麦特性和麦芽的后续改性。
麦芽粉组成主要通过使用麦芽粉箱或其他筛分系统手动监控。通常在磨机运行时,从磨机底部沿辊子长度获取多个麦芽粉样品。这些样品通常在麦芽粉分离箱(1.98毫米和0.212毫米筛网)(Stevenson Reeves, Ltd., 爱丁堡,苏格兰)(或类似的筛组)中摇动进行单独分析,每个筛分级分的重量给出谷壳、中间颗粒和面粉组分的相对比例。Dolan(2003)建议,对于传统糖化桶,充分改性的蒸馏麦芽的最佳麦芽粉组成为20%谷壳、70%粗粒(中间颗粒)和10%面粉,而半过滤桶或过滤桶的麦芽粉可能更细。然而,糖化桶具有不同的特性,实际的麦芽粉规格在很大程度上取决于所使用设备的范围。过多的细面粉(>10%)可能会导致麦汁分离问题。
一些权威人士引用的筛号范围比蒸馏厂传统使用的简单麦芽粉分离器更广。Briggs等人(2004)强调了酿造中常用的EBC/Pfungstadt筛分系统,该系统提供了与传统和过滤桶相关的更精确的筛网尺寸范围。表6.4给出了差异比较,并显示了过滤桶通常使用的更细研磨。(酿造)糖化过滤器的比较数据显示麦芽粉更细。
| 筛号 | 筛网(mm) | 组分 | 糖化桶 | 过滤桶 | 糖化过滤器 |
|---|---|---|---|---|---|
| 1 | 1.27 | 谷壳 | 27 | 18–25 | 8–12 |
| 2 | 0.26 | 粗粒 | 9 | 8–<10 | 3–6 |
| 3 | 0.15 | 细粒I | 24 | 35 | 15–25 |
| 4 | 0.07 | 细粒II | 18 | 21 | 35–45 |
| 5 | 0.04 | 面粉 | 14 | 7 | 8–11 |
| 托盘 | — | 细面粉 | 8 | 11–<15 | 12–18 |
表6.4 与糖化槽和传统糖化过滤器相关的麦芽粉碎成分
来源:改编自Briggs等人(1981和2004)。
筛子的排列(表6.4)更精确地指示了来自磨机的麦芽粉组成。尽管这些值与仅分离粗、中、面粉组分的传统蒸馏厂麦芽粉分离箱之间存在一些重叠,但很难精确关联它们。大致而言,粗/谷壳组分与筛号1上的物质相似,而中间颗粒将是筛号2、3、4和5的总和,面粉近似于通过最小筛号(5)的物质。
然而,这两个系统之间没有特定的对应关系,对于蒸馏厂来说,重要的是一致地应用其中一个系统,以了解单个蒸馏厂的必要性能限制,以及蒸馏厂自己在将麦芽粉组成与特定糖化桶的操作要求相匹配方面的经验。这样做将使蒸馏厂能够有效地应对麦芽供应的变化,确保蒸馏厂的糖化桶在可用设备的范围内高效且一致地运行。
研磨过程
在进入蒸馏厂工艺之前,大麦芽从麦芽仓转移到较小的麦芽料斗,经过进一步的去石机和筛网去除任何残留的石头、碎屑、茎秆和灰尘后,从料斗输送到磨机。这通过称重陷阱完成,称重陷阱通过将固定重量的麦芽(通常约25至50公斤)倾倒入磨机进料口来反复卸料。通常,蒸馏厂会设置固定数量的“倾倒”(或“批次”)以提供糖化所需重量的麦芽粉。通常,每次糖化约10吨,但这可能因单个蒸馏厂设备的尺寸和容量而有很大差异。四辊磨机的典型吞吐量约为每小时每毫米辊长2至6公斤(Briggs等人,2004)。
在辊式磨机中,谷物通过几组辊子时被压缩。辊式磨机的使用提供了麦芽粉的相对温和分离,并使谷壳部分相对不受损坏,这使得它们特别适合在传统或过滤桶中需要分离麦汁的工艺中使用,因为谷壳在糖化过程中能够充当过滤床(Kelsall和Lyons,1999)。
不同蒸馏厂的研磨设备可能不同,但图6.7所示的四辊类型的变体被普遍使用。一些蒸馏厂可以使用六辊磨机,其用途更广泛,可以提供更细的麦芽粉,更适合大型蒸馏厂(和啤酒厂)。Dolan(2003)认为,后者对于处理现代充分改性的麦芽不是必需的。
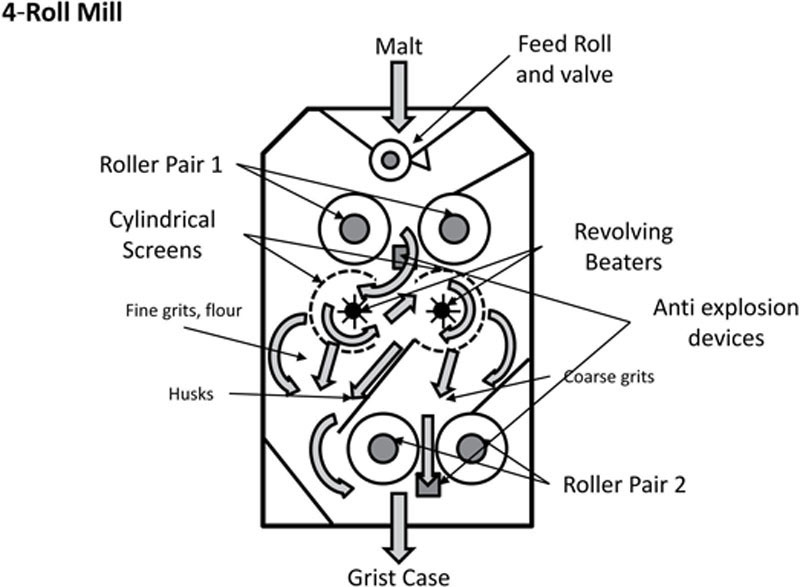
在四辊磨机中,麦芽通过进料辊进入磨机,进料辊引导流向,使单个谷物“端对端”通过一对可调弹簧加载辊(通常为凹槽),辊子直径通常约为250毫米,最大工作长度约为1500毫米。主驱动辊通常在250至500转/分钟之间运行。这些辊子旨在沿谷物长度压碎谷物,而不会严重损坏谷壳部分。第一组辊子之间的间距设置为提供适当的初始研磨(1.3至1.9毫米)以压碎麦芽颗粒;应定期检查辊子的磨损情况并确保它们平行。有时两个辊子都被驱动,但在某些情况下,一个可能是从动辊,由谷物和驱动辊之间的摩擦力驱动。辊子可能以不同的速度运行,以提供剪切力,使谷物更有效地研磨。
从第一对辊子开始,破碎的麦芽粉部分分离成麦芽粉和谷壳组分,然后通过第二对辊子,第二对辊子的间距设置得更近(0.3至1.0毫米)。在一些设计中,破碎的麦芽粉通过一组搅拌器,搅拌器将麦芽粉组分引导通过筛网,将面粉和细粒与粗粒分离,然后将粗粒引导通过第二对辊子进行进一步粉碎。谷壳组分几乎完整地通过搅拌器落下,绕过第二组辊子,从而在它们与麦芽粉箱中的其他麦芽粉汇合之前最小化任何进一步的损坏。
筛网的排列使得通过它们进入第二组辊子的粗粒和细粒的比例可以变化,以微调最终的麦芽粉组成。在一些磨机中,使用振荡平板筛来提供类似的结果(Briggs等人,2004)。磨机还包含防爆装置,这些装置是设置在辊子下方的架子或挡板,旨在扑灭任何火花,并将谷物通过磨机时产生的灰尘引起爆炸的风险降至最低。当麦芽粉被研磨时,它被收集在麦芽粉箱中,从那里被转移到糖化机并最终进入糖化桶。
调节
在某些情况下,调节可用于通过在到达磨机之前用少量低压蒸汽湿润谷壳材料短时间(30秒至1分钟)来软化和降低其脆性。这种精心控制的处理可以改善谷壳组分的保留,而不会影响淀粉质胚乳的研磨特性。它还可以提供其他好处,例如改善麦汁流出时间,并通过允许过滤桶装载更深来改善其性能特性,因为它会降低床密度并增加孔隙率(Briggs等人,2004)。还建议调节后的麦芽将具有更好的性能,具有更高的提取物收率和衰减率以及更快的糖化速度(Briggs等人,2004)。使用调节后的麦芽需要调整磨机以提供更近的辊隙以实现最佳提取。调节还会增加废谷物的体积。
锤式研磨
冲击研磨,使用锤式磨机等设备,很少被(传统)麦芽蒸馏厂使用,它们通常使用相对粗的麦芽粉。然而,这些在谷物蒸馏厂中使用更广泛,在那里必须使用相对细的研磨来处理未发芽的谷物。一个应用是在使用麦汁过滤器的麦芽蒸馏厂系统中。该系统需要非常细的麦芽粉才能高效运行。目前,这些在苏格兰麦芽威士忌的生产中很少使用,但在撰写本文时,至少有一家蒸馏厂正在运行糖化过滤器。
糖化
糖化是麦芽蒸馏厂工艺的阶段,其中麦芽粉与液体混合、水合并在特定温度(通常为63.5至64°C)下浸泡,使淀粉糊化,麦芽酶能够有效地将其水解为可发酵糖。这些糖被溶解并提取到麦汁中,麦汁与谷物分离,冷却,并在接种酵母后转移到发酵罐。在第一遍水排出后,糖化液用更高温度范围(通常为70至90°C)的进一步水提取。
糖化桶类型
糖化是使用三种主要类型的糖化桶之一进行的分批过程。传统糖化桶(有时仍在较旧的蒸馏厂中发现)是通常由铸铁或钢制成的圆柱形容器(Bathgate,2003)(图6.8)。这个相对粗糙的系统最初没有绝缘或盖子,具有大型旋转桨叶来混合糖化液和犁耙,以在糖化后去除废谷物( draff )。在一些非常古老的传统糖化桶中没有犁耙,必须用铲子手工排出废谷物。糖化桶有一个假底或甲板,带有可移动的开槽炮铜或钢板或楔形金属丝,支撑在底部上方以支撑糖化床。多年来,原来的开放式糖化桶被铜或钢盖覆盖,并至少部分绝缘以保留更多热量。最初,传统的桶没有任何喷洒系统(Dolan,2003),但最终安装了带有相对粗糙喷洒系统的旋转喷洒臂,因此糖化液可以用热水喷洒。
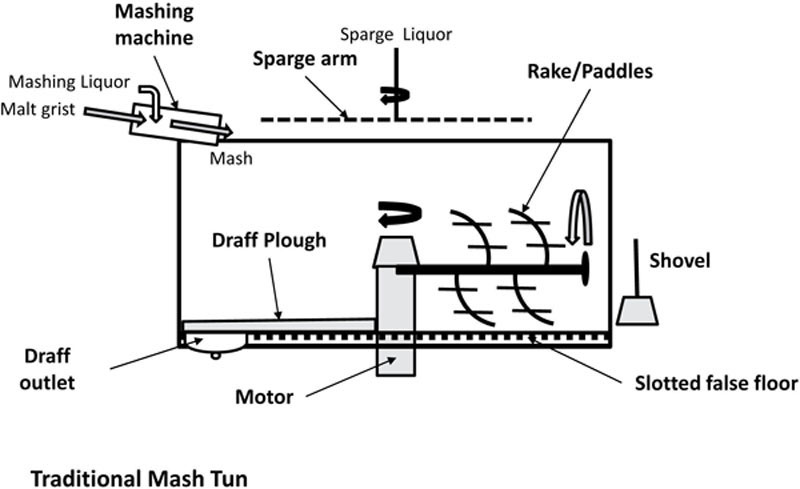
传统的桶将使用浸泡糖化系统,其中糖化液在排干至干燥之前静置固定时间段(通常长达1小时)。然后将谷物用更高温度(通常为70至75°C)的第二遍水提取,并再次用>80°C的第三遍水提取并排干至干燥。一些传统糖化桶使用约90°C(或更高)的第四遍水。在某些情况下,第三和第四遍水将合并以在相对较高的温度(>85°C)下提供复合第三遍水。一般来说,每遍水的量可能有很大差异,具体取决于使用的大麦芽量和目标原始比重,但第一、第二、第三和第四遍水的大致比例被认为是每糖化一吨麦芽4:2:2:4立方米(Bathgate,1989;Dolan,2003)。传统糖化桶的主要缺点是糖化过程相对缓慢且效率低下,因为麦汁流出被中断以允许添加每遍水和随后的混合以重新制作糖化床。传统糖化桶最初设计为在相对较低的原始比重下工作,范围从1040至1050°IOB(10至13°柏拉图)(Dolan,1976)。在现代使用中,更典型的是1055至1060°(14至15°柏拉图)的更高麦汁原始比重。现代过滤和半过滤桶能够常规在更高的比重(1065至1070°;16至18°柏拉图)下工作,至少有一家蒸馏厂的目标原始麦汁比重高达1080°(20°柏拉图)。传统糖化桶在某些蒸馏厂中仍然很重要,因为它们通常被认为提供独特的特性,并有助于苏格兰麦芽威士忌生产的传统形象。
现代过滤和半过滤系统效率更高且更灵活。这些属性在2010年代不断扩大的生产条件下尤为重要,因为它们允许蒸馏厂在不增加额外蒸馏厂容量的情况下有一些增加生产水平的灵活性。麦芽蒸馏厂的全过滤系统概念与啤酒厂不同,啤酒厂通常指的是糖化液在单独的容器中混合和浸泡,然后转移到过滤桶中分离麦汁的系统(O’Rourke,2003)。在麦芽蒸馏厂中,全过滤桶是一种高性能糖化桶,其中容器中的技术足够灵活,可以高效地提供非常高的提取物和良好的流出特性。
目前麦芽蒸馏厂使用的最重要的糖化桶类型可能是半过滤桶(图6.9),Dolan(2003)将其定义为“使用具有传统浸泡糖化协议的过滤桶”。然而,实际上,半过滤桶的范围比这更广泛,有效地涵盖了传统桶和全过滤系统之间的所有内容。过滤(或半过滤)桶与传统桶的主要区别在于,过滤系统旨在比传统桶更快、更高效地输送过滤后的麦汁。过滤桶中的床深度通常较浅,在0.5至1.0米范围内,而传统桶中的床深度要高得多(1.0至1.5米)。过滤桶没有传统的耙子,而是装有一组带有与每个叶片成直角设置的角度叶片(鲨鱼鳍)的刀具;它们可以对糖化床施加额外的温和压力,这有助于从糖化床中提取更多的液体麦汁。耙子可以升高和降低以维持流出速率。更先进的版本可能有几个前进和后退齿轮,以增加压力或在必要时帮助提升床层,如果存在严重的排水问题。与传统桶一样,糖化桶底部有开槽的炮铜或钢板或楔形金属丝。更现代的半过滤(和过滤)桶使用带有过滤槽的不锈钢板,在某些情况下这些板是固定的,需要某种板下清洁以保持它们不受污染。
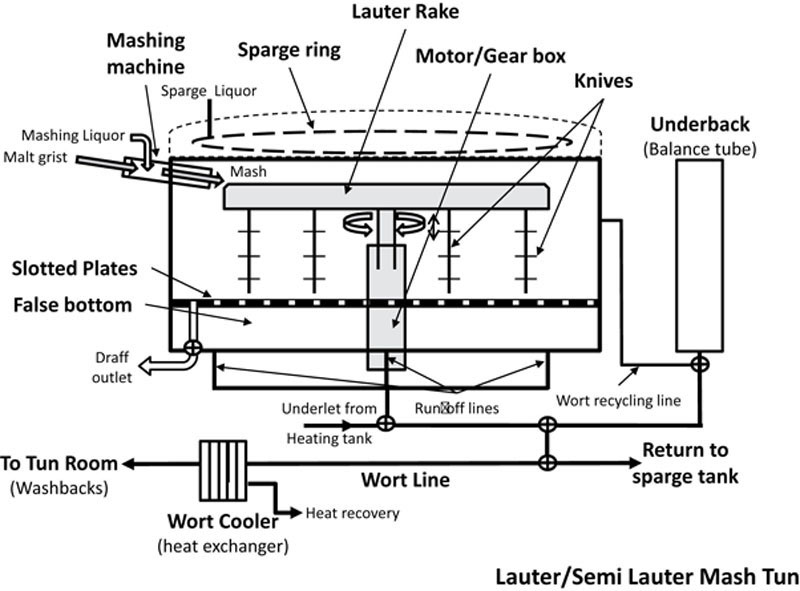
喷洒通过设置在喷洒环内的一系列高效喷洒喷嘴进行。这些喷嘴旨在输送非常热的水的细雾,这将有助于从糖化液中高效洗提可溶性物质,例如可发酵糖、淀粉、低聚糖和糊精。通常,在过滤桶中糖化后,废谷物相对干燥,仅含有极少量的残留提取物(0.5至1%重量)。由于过滤桶设计为使用更细的研磨,因此它将比传统糖化桶产生更好的提取物收率。
用半过滤桶糖化
麦芽蒸馏厂通常有两个主要的加热罐,其中一个将包含清洁水(即水箱),另一个包含喷洒液(即喷洒罐),这是来自先前糖化的弱(第三遍)麦汁。一些蒸馏厂将每个罐分开,而其他则互换使用。必须定期清洁这些罐,以避免细菌污染的积累,这会对生产效率产生负面影响。
弱麦汁通常从糖化桶/底槽的麦汁管线直接以高温返回喷洒罐。喷洒液通常保持在相对较高的温度(>70°C)以保持其不受感染并防止液体变质。由于喷洒液在接近最终糖化温度(可能约为90°C)的温度下循环回罐,因此在送回糖化桶之前必须冷却。这可以通过向加热罐中添加冷水来实现,或者更有效地通过使喷洒液通过热交换器来降低温度,因为它返回喷洒罐。这允许更好的温度控制,最大限度地减少添加到罐中的额外水量,并允许蒸馏厂在更高的比重下运行。从喷洒液中移除的热量然后可以在工艺的其他地方使用。为了节省能源,一些蒸馏厂可能在较低的(最终)喷洒温度下运行,这意味着在开始下一次糖化之前对冷却的需求较少。通常会监控喷洒罐中的温度。这可用于计算添加麦芽时的糖化温度,因此当糖化液进入糖化桶时达到正确的温度。
底部注水
糖化的第一阶段称为底部注水,包括向糖化桶中添加热糖化液以覆盖板的表面。这具有预热糖化桶板的效果,并有助于最小化糖化液与板接触时的任何冷却。薄液层的存在还有助于防止糖化过程中细颗粒通过糖化桶底部。作为底部注水添加的液体体积将因每个单独糖化桶的设计和尺寸而异。
糖化进料
大多数麦芽蒸馏厂仍在使用传统Steel糖化机的变体来将麦芽粉与糖化液混合(图6.10)。最终,像涡流混合器(图6.11)这样的更现代变体,没有移动部件,将在麦芽蒸馏厂和啤酒厂中得到越来越多的使用。
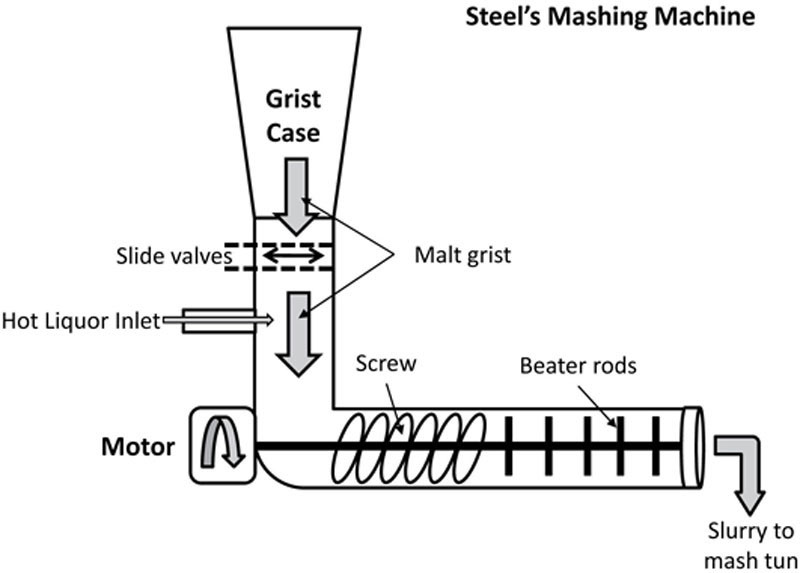
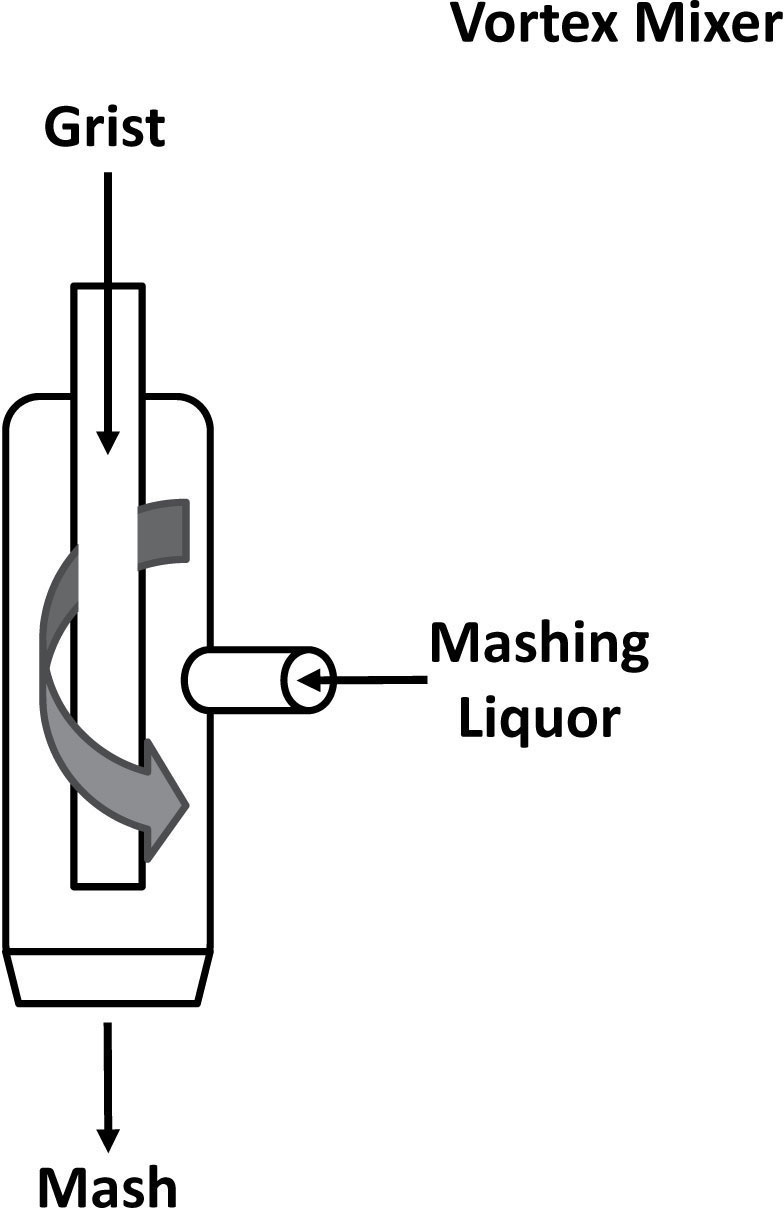
在Steel糖化机中,麦芽粉从麦芽粉箱通过滑阀添加,并与通过热液入口进入的热液混合。当麦芽粉撞击热液时,它通过沿着带有一系列搅拌器的混合螺杆彻底混合,搅拌器将糖化浆液驱动到糖化机末端的喷口。浆液的撞击温度和最终温度对于确保正确进行糖化至关重要。在涡流混合器(图6.11)中,使用相同的基本原理,麦芽粉与注入的糖化液混合以提供涡流,当糖化液通过容器时,涡流有效地混合糖化液。
最初,热液的温度通过添加冷水手动控制,以调整撞击温度(通常为68至70°C)以达到正确的糖化进料喷口温度(通常为63.5至64°C),该温度将从设置在糖化机末端的传感器显示。在更现代的蒸馏厂中,这更可能通过使用反馈回路自动控制。一些蒸馏厂可能旨在通过使用热交换器将喷洒液直接调节到正确的撞击温度来最小化冷水的输入。在整个糖化进料过程中,糖化温度保持在63.5至64°C至关重要。高于65°C的温度将导致重要麦芽酶的快速失活,并导致淀粉和糊精的水解不充分,从而导致发酵不完全。当糖化进料完成时,操作员通常记录最终糖化温度和糖化桶中的液位。通常,当糖化进料完成时,喷洒罐将或多或少是空的,然后将用淡水填充并加热到第三遍水的温度。
糖化进料需要20到30分钟,具体取决于添加的麦芽粉量和糖化桶的大小。最初,糖化液在糖化进料过程结束前不进行耙动,因为过早耙动会导致细颗粒被迫通过糖化桶槽,这可能导致随后的麦汁流出问题。
当糖化进料完成时,快速旋转耙子以形成床层,然后让其沉降约10分钟,然后小心打开到底槽的阀门并松弛到底槽(或静液压平衡管),底槽将通过重力填充,直到液位与糖化桶中的液位平衡。底槽保持糖化液的静液压平衡,防止在麦汁排出时将其吸到糖化桶板上。底槽中的麦汁液位通常平衡以反映糖化桶中的液位,任何差异都是麦汁分离问题的良好指标。
由于过滤桶中使用更细的麦芽粉,细颗粒可能会通过过滤槽逸出,一些蒸馏厂更喜欢通过小心地将底槽中的少量麦汁循环回糖化桶(vorlaufing)来去除它们。完成后,开始流出,麦汁被缓慢泵过麦汁冷却器,将其冷却至正确的接种温度(通常约16至19°C),然后接种酵母,然后送到调酿室的发酵槽中进行发酵。酵母可以在麦汁进入发酵槽之前注入麦汁管线,这反映了使用奶油状和/或繁殖酵母的现代实践,或者可以作为袋装(压榨)酵母直接添加到发酵容器中。
当开始流出时,缓慢耙动糖化液。最初,糖化液随着耙子轻轻漂浮,但随着漂浮床与板接触,逐渐减慢。刀具缓慢而温和地切入床层,逐渐从糖化液中挤出液体。
当糖化床表面开始显现时,操作员通常会开始通过喷洒喷嘴添加第二遍水。与简单地通过糖化喷口添加相比,这相对耗时,但具有通过糖化床均匀洗提麦汁同时逐渐升高糖化温度的优点。不同的蒸馏厂可能会改变他们添加第二遍水的方式,但重要的是,在发酵罐(发酵槽)中有足够的麦汁供应足够的酶以将麦汁中的糊精完全转化为可发酵糖并确保发酵完成之前,糖化温度不要升高得太快。
在糖化过程中,必须在流出速率、发酵槽中的麦汁水平和实现所需生产水平的可用时间之间保持仔细平衡。实际上,蒸馏厂将利用他们的经验开发适合蒸馏厂限制的系统,并提供一致且可重复的程序。这可能仅基于固定的流出时间和/或流速。在更现代的工厂中,将监控来自糖化桶的流量,并且一旦收集到特定体积的麦汁,将在设定点添加第二遍水。关于第二遍水添加点的精确性对于实现每次糖化的一致原始比重至关重要。此外,第二遍水的添加时间和速率对于允许糖化温度随着热液洗提通过糖化液而逐渐升高至关重要。
如果使用适当的过滤系统,在添加第二遍水时,排水通常会不间断地进行,然后继续直到发酵槽装满。第二遍水通常是来自加热罐的清洁热水(85至95°C),但根据容器的相对尺寸,它可能包含糖化进料阶段剩余的喷洒液。第三遍水通常是从热水罐以高温(85至95°C)添加的清洁水;一旦发酵槽已完全填充到所需水平,通常会将其添加到糖化液中,此时麦汁流简单地转移回热液罐。用热水持续喷洒将热量保留在床层中,并允许糖化温度稳定上升至最高温度,可能高达95°C,尽管一些蒸馏厂可能选择在较低温度(例如85°C)下运行以节省能源。在后期阶段,耙子的速度将增加。与糖化温度的升高一起,这具有从糖化液中高效洗提提取物的效果,并且还有助于增加流出速率。每个糖化桶将有自己的协议,该协议已适应单个蒸馏厂的容量和生产要求。
在一些半过滤系统中,与传统桶一样,在添加第二遍水时停止排水,并在重新制作糖化床时重新开始。在这种情况下,第二遍水在较低温度(通常约70至75°C)下添加,排水重新开始直到发酵槽装满。在发酵槽装满后停止流出后,添加第三遍水(有时是第四遍水)。由于喷洒可能相对缓慢,为了节省一些时间,一些蒸馏厂可能会通过糖化喷口部分或全部添加最终水,但这通常需要重新制作糖化床。第三遍水流出在任何温度调整后被引导至(喷洒)加热罐;然后将加热罐填充到下一次糖化所需的水平。
当糖化完成时,停止排水,废谷物(draff)从糖化桶中排出, either 通过使用可伸缩犁耙 or 通过调整耙刀将它们引导通过废谷物出口。废谷物通常出售给当地农场作为动物饲料,送到中央副产品加工厂掺入深色谷物中,或添加到厌氧消化饲料或其他废物回收处理中。
糖化过程中的一个关键考虑因素是平衡糖化过程中使用的液体,以避免麦汁浓度的波动,并确保没有液体短缺或需要丢弃的过量液体。
糖化过滤器
糖化过滤目前在酿造中常规使用,但在麦芽蒸馏厂中尚未受到普遍青睐,尽管已知一家苏格兰威士忌蒸馏厂现在正在运行糖化过滤器。Bathgate(2003)提到该技术过去曾被使用,但与使用传统和半过滤桶的常规糖化系统相比,没有显示出主要优势。然而,该技术继续发展,因此预计它可以提供性能的进一步改进。
糖化过滤器与单独的糖化/转化容器一起使用,在糖化/转化容器中,糖化液在转移到过滤器进行麦汁分离阶段之前,在正常糖化温度(64至65°C)下混合并保持,以使麦芽酶将淀粉转化为可发酵糖。与糖化桶不同,谷壳组分不需要提供过滤床,现代高压糖化过滤器的使用允许使用更细的锤磨面粉。这为糖化过滤器提供了额外的灵活性来处理否则难以加工的大麦芽。此外,由于过滤层通常非常窄(4至6厘米),过滤速率更快,麦汁收集时间可能比糖化桶更短。然而,为了使糖化过滤器高效工作,它必须完全填充,并且只能处理固定体积的糖化液,除非安装了笨重的 blanking plates。
单个糖化过滤器各不相同,但通常由包含在腔室模块中的两种主要单元类型(膜支撑和过滤板)组成(图6.12)。其核心是膜框架,这是一个薄的带槽板,在板的任一侧支撑两个弹性隔膜,通常由聚丙烯或橡胶制成,通过控制气压可以充气或放气。膜框架夹在两个支撑过滤片的板之间,它们之间的空间提供了一个狭窄的腔室,糖化液保留在其中。可以对隔膜充气以向糖化液施加额外压力,以驱动麦汁通过过滤片。麦汁通过细孔聚丙烯过滤片过滤,当麦汁被收集时,过滤片保留谷物。大量这些单独的模块(通常为10至60个,取决于糖化容量)被压缩在一起组成完整的糖化过滤单元。
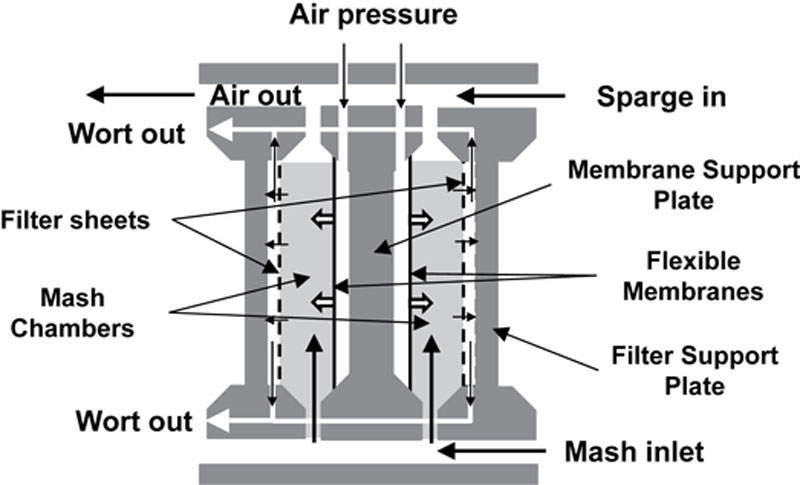
O’Rourke(2003)和Briggs等人(2004)描述了酿造中典型糖化过滤器的操作。总体原理与苏格兰威士忌生产相同。过滤器被预热,糖化液从底部填充以减少糖化液曝气,允许糖化腔室均匀填充并排出空气。继续输送糖化液,直到所有腔室都被填充,此时关闭通风口并打开麦汁出口。施加到隔膜/膜与其支撑物之间空间的气压允许隔膜膨胀并将麦汁挤压通过过滤片,液体在过滤器顶部和底部的麦汁出口处收集。然后可以将麦汁流合并、冷却,并以正常方式泵送到发酵罐。随着过滤的进行,逐渐释放隔膜的压力,并通过从装置顶部以更高温度(通常为75至78°C)泵送第二遍水来喷洒糖化液,以便将其冲洗通过谷物,置换剩余的麦汁,并在过滤后收集为弱麦汁。一旦喷洒完成,进一步压缩糖化液以收集最后的麦汁部分。通常,强(第一遍)麦汁进入发酵过程,而弱(第二遍)麦汁被返回单独的罐或下一次糖化的糖化容器。典型的60板麦汁过滤器(用于酿造)可容纳约10.5吨大麦芽(Briggs等人,2004)。第一遍麦汁浓度很高,比重约为1085至1090°(21至22°柏拉图)。
当糖化完成时,过滤器打开,谷物通过螺旋输送机排出到正常的副产品流中。过滤过程非常高效,将导致更干燥的废谷物,这将减少废水处理系统的负荷。循环时间通常约为2小时(Briggs等人,2004)。随着过滤片变脏,麦汁流动的阻力增加,需要定期用清水冲洗过滤器,定期使用苛性清洁剂和可能的次氯酸盐(Briggs等人,2004)。如果谷物粘稠,必须从过滤片上物理去除残留物(O’Rourke,2003)。
糖化过滤器的两个优点是它提供了额外的灵活性来处理否则难以加工的麦芽,并且其处理来自细磨面粉的麦汁的能力使该过程能够适应更广泛的材料,如无壳大麦芽。糖化过滤器可以提供高效的提取物回收——约99.5%的实验室提取物(Briggs等人,2004)——以及更快的周转时间。此外,糖化过滤器为自动化提供了更多空间,并可以减少用水量和废水产生。
另一方面,与过滤桶相比,该系统的运行成本可能更高(Briggs等人,2004),并且需要单独的糖化容器和额外的设备来混合糖化液并将其转移到过滤器。与大型糖化桶相比,一些糖化过滤器的容量相对较小,可能需要多个循环来填充发酵槽。一般来说,尽管糖化过滤器的移动部件较少,但需要定期维护、清洁和更换过滤片和隔膜。有时需要中断生产运行序列进行清洁(Briggs等人,2004)。
尽管废谷物比传统废谷物干燥得多,这有一些优点,但副产品可能更难处理。此外,由于过程中排出空气的方式,与传统麦汁相比,麦汁的曝气较少且脂肪酸含量较低(Briggs等人,2004)。这可能会影响发酵效率并影响最终烈酒的质量,但在酿造中可以克服,因为通往发酵的麦汁通常会被充氧。
到目前为止讨论的技术展示了几乎所有当前麦芽蒸馏厂使用的工艺的主要组成部分。该过程的大部分仍然是传统的,但从技术公司那里吸取了关于将工艺与水和能量回收系统以及副产品利用相结合的现代方法的教训,特别是在现代扩建和新建蒸馏厂中。当考虑谷物蒸馏厂的设计和操作的最新发展时,这一点尤为明显。
谷物蒸馏厂加工与原理
多年来,为了提高效率,谷物烈酒生产的基本工艺和技术不断发展。这些变化包括原材料和环境保护法规,以及实现可持续发展目标的现代举措,如减少碳足迹、水和能源使用,以及降低环境排放。近年来,通过引入低温加工,人们越来越重视降低能源需求。与此密切相关的是,在生产过程中加强了能量回收系统和副产品流的整合。其他主要变化包括提高麦汁原始比重,有时超过1080°(20°柏拉图)以减少用水量和提高产量,以及从压榨酵母转向奶油酵母。后者虽然增加了资本支出,但改善了酵母管理并更好地控制了酵母接种率。
谷物蒸馏,即未发芽谷物的加工,有两个主要目标:(1)从谷物中释放淀粉;(2)将这些淀粉转化为可发酵糖。通常,第一个目标是通过在高温或高压下蒸煮谷物来实现的。这会使淀粉糊化,从而可以释放和溶解。来自高酶大麦芽的酶然后可以将淀粉转化为可发酵糖,这些糖又被酵母发酵成酒精。在低温工艺中,淀粉不会以同样的方式糊化;相反,通过细锤磨将颗粒破坏,使其更容易被α-淀粉酶分解,α-淀粉酶可以降解天然淀粉并降低糊化温度(Lynn等人,1997,1999)。
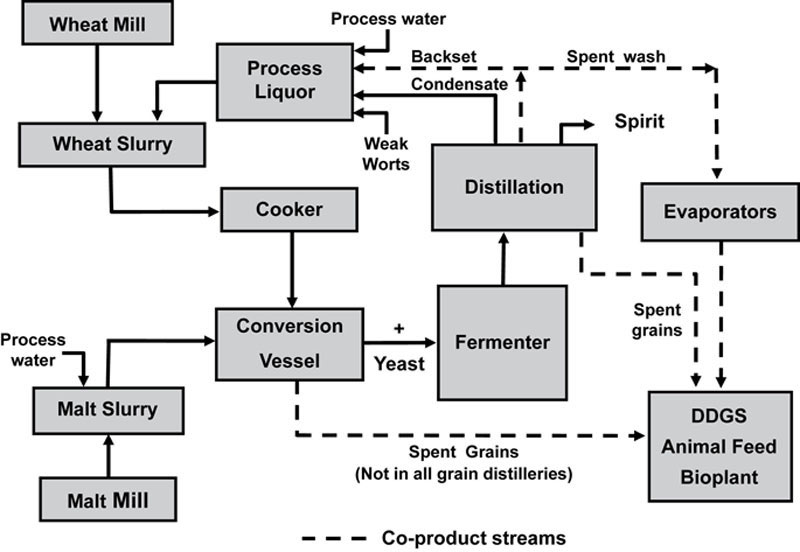
图6.13中的流程图展示了典型谷物蒸馏厂工艺的主要特点。一般来说,该工艺的主要特点适用于高温和低温工艺。图6.13代表了苏格兰威士忌行业中谷物蒸馏厂谷物加工的概括性概述;实际上,该工艺的每个部分都有广泛的工艺选择。表6.5总结了目前苏格兰威士忌谷物蒸馏厂使用的一些选项,并说明了苏格兰谷物威士忌生产中采用的各种工艺。
| 工艺步骤 | 选项范围 |
|---|---|
| 工艺 | 批次、半连续 |
| 谷物 | 小麦、玉米 |
| 研磨 | 锤式磨机(粗/细)、粉碎机、辊式磨机(粗碎) |
| 工艺液 | 水、回料(釜残液)、冷凝水、弱麦汁 |
| 蒸煮 | 高温/高压、高温常压、低温 |
| 转化 | 干(白)高糖化力(DP)麦芽、绿麦芽(商业生产) |
| 麦汁分离 | 通常无,粗麦汁筛 |
| 原始比重 | 1060°–1085°(15–21°柏拉图) |
这些选项各有优缺点,每个蒸馏厂的系统设计都符合各自公司的目标和宗旨。这些主要是在生产需求的背景下,基于自身在工厂设计和技术方面的经验发展而来的。在某些情况下,它们可能以国际上开发的其他谷物烈酒生产工艺的特点为模型。
大多数谷物蒸馏厂继续运行批次蒸煮工艺,主要使用相对较高的蒸煮温度(95至145°C)。然而,近年来,随着威士忌生产的扩张,有一种转向更大批次或半连续操作的趋势。最近新建的谷物蒸馏厂设计为在更低的加工温度下运行,但传统高温工艺的一些特点至少部分保留,以维持蒸馏厂的整体能量平衡,并允许热回收和传输系统高效运行。
小麦仍然是苏格兰威士忌谷物蒸馏厂使用的主要谷物,尽管玉米(玉米)至少在一家蒸馏厂中仍扮演重要角色。一般来说,大多数谷物蒸馏厂会用锤式磨机研磨谷物,尤其是在使用低温蒸煮工艺时。从技术上讲,没有麦汁分离阶段,现在几乎所有谷物蒸馏厂都通过处理未过滤的麦汁来运行。在某些情况下,麦汁可能会通过粗筛系统去除任何粗碎屑,这些碎屑可能会在工艺的后续阶段产生下游影响。
一个根本且日益重要的变化是高度集成的水和能源管理系统的出现,以减少整体水和能源使用。这些系统通过在工艺的各个部分重复使用热交换工艺水,以及将某些液体副产品流作为工艺液(例如回料)进行循环来管理。这方面的另一个方面是,为了减少用水量和提高谷物产量,一些谷物蒸馏厂正在逐步转向更高比重的操作,原始比重从约1060°(16°柏拉图)上升到某些情况下高达1075至1085°(19至21°柏拉图)。
尽管谷物蒸馏厂使用的工艺细节发生了许多变化,但总体而言,前一版(Bringhurst等人,2003)中概述的谷物蒸馏厂加工原理仍然相关。
传统蒸煮工艺
Kelsall和Lyons(1999)将蒸煮工艺定义为从谷物与液体混合开始,到将糖化液输送至发酵罐结束的过程。实际上,这一过程由四个部分组成:研磨、蒸煮、排污和转化。
研磨
在谷物蒸馏厂处理谷物时,进料后的第一个阶段通常是研磨谷物,尽管有时也会处理整粒谷物。研磨方式的选择主要取决于其成本与通过缩短蒸煮时间节省的能源之间的平衡(Piggott和Conner,1995),如今谷物的锤式研磨已成为常态而非例外。Kelsall和Piggott(2009)回顾了谷物蒸馏厂使用的一些研磨选项,总体原则并未改变。
研磨的主要目的是破坏谷物的结构,以便在后续蒸煮过程中促进水分渗透到谷物胚乳中(Kelsall和Lyons,1999)。精细研磨还具有机械破坏淀粉颗粒的作用,这有助于水分的吸收(Evers和Stevens,1985),促进淀粉从谷物蛋白质基质中的机械释放,并降低糊化温度(Lynn等人,1997)。研磨还有助于分解胶质(如阿拉伯木聚糖和β-葡聚糖)和其他细胞壁物质,并在后续过程中促进蛋白质的溶解。
如前所述,在苏格兰威士忌行业中,主要使用两种类型的磨机:辊式磨机和锤式磨机。也使用过销式磨机(粉碎机)。在某些情况下,可以采用湿磨,但主要用于处理如下所述的绿麦芽。辊式磨机通常用于麦芽威士忌的生产,但也可用于谷物蒸馏;它们特别适合研磨小颗粒谷物,如大麦芽和小麦。在辊式磨机中,谷物通过几组辊子时被压缩,通常是三组两辊(六辊磨机)。
锤式磨机通常用于谷物蒸馏厂,因为这些磨机可以将谷物破碎成均匀的面粉,相对容易处理。锤式研磨还使谷物蒸馏厂能够使用短期蒸煮和糖化工艺,特别适合连续工艺(Wilkin,1983)。
在锤式磨机中,整粒谷物(玉米、小麦)被送入研磨室,并通过多个旋转的锤子粉碎成均匀的面粉。通过使用固定尺寸的筛网(通常为0.5至2.5厘米)来控制麦芽粉的大小,该筛网会保留较大的颗粒,直到它们被破碎成均匀的尺寸(Kelsall和Lyons,1999)。使用锤式磨机时,重要的是不要将谷物研磨得太细。这可能导致结块,使少量未加工的淀粉通过该过程。此外,研磨过细会对蒸馏后釜残液(废洗液)的固体含量产生不利影响,并给蒸发器增加额外负荷,从而导致潜在的下游加工问题。
研磨的细度也会影响该过程的酒精产量。如果研磨太粗,在加工过程中淀粉可能无法完全糊化,据报道,粗度增加约0.2厘米会导致酒精产量减少约7.5%(Kelsall和Lyons,1999)。
谷物蒸馏厂通常更喜欢在加工前研磨谷物,尽管至少有一家蒸馏厂仍在处理整粒谷物;然而,锤式研磨现在是常规做法。尽管过去使用整粒谷物是有效的(Bathgate,1989),但延长蒸煮时间会带来成本损失。然而,使用整粒谷物的优点是有可能减少褐变反应的程度,这可以提高酒精产量(Bathgate,1989)。
现代低温工艺要求谷物被相对精细地研磨,因为这会充分破坏淀粉颗粒,使淀粉在较低温度下糊化(Lynn等人,1997)。此外,使用小比例的预麦芽和回料可用于促进酶水解,并确保存在足够的游离α-氨基氮(FAN)来支持发酵。
蒸煮原理
蒸煮过程的主要功能是破坏连接淀粉分子的氢键,并将淀粉从蛋白质基质中分离出来,从而破坏其颗粒结构并将其转化为胶体悬浮液(Kelsall和Lyons,1999)。在玉米等谷物中,糊化温度远高于参与将淀粉转化为可发酵糖的酶所能发挥作用的温度(62至67°C)(Palmer,1986)。因此,在利用淀粉之前,通常必须蒸煮谷物(Wilkin,1989)。蒸煮的程度在很大程度上取决于所使用的谷物。这通常由糊化温度决定。玉米的糊化温度远高于小麦,必须在更严格的条件下蒸煮(Bathgate,1989)。当淀粉糊在100至160°C下蒸煮时,淀粉分子会真正溶解(Swinkels,1985)。
尽管有些蒸馏厂偶尔仍会使用玉米,但自1984年以来,用于生产苏格兰谷物威士忌的主要谷物一直是小麦(Brown,1990)。从理论上讲,小麦似乎几乎不需要或不需要额外蒸煮,但实际上,蒸馏厂的经验表明,蒸煮小麦可以更好地利用淀粉并更完全地分解谷物(Bathgate,1989)。此外,由于该过程的经济性在未来可能会促进大规模回归玉米加工,许多蒸馏厂保持了加工玉米和小麦的能力,因此至少部分保留了传统的蒸煮工艺,而不是进行重大改变。通过不完全实施Wilkin(1989)和Newton等人(1995)建议的冷蒸煮工艺,这些蒸馏厂可以应对原材料市场的变化。此外,谷物蒸馏厂的现代设计集成了热回收和废水减少系统,这些系统与为谷物高温蒸煮设计的技术有着内在的联系。
小麦的问题之一是它含有大量的细胞壁物质,如阿拉伯木聚糖,这可能在加工过程中以及蒸馏后废谷物/洗液的回收过程中对蒸馏厂的产量造成严重问题。蒸馏厂的实际观点是,这个问题可以通过蒸煮来缓解。然而,现代副产品处理系统的出现,如厌氧消化(AD)和其他不需要传统蒸发系统的沼气生成系统,也可能为这些问题提供部分解决方案。
尽管有时在谷物蒸馏厂中使用未发芽大麦,因为它可能比其他谷物便宜,但由于蒸煮过程中存在高水平的β-葡聚糖以及副产品回收过程中,它会导致非常严重的粘度问题(Bathgate,1989;Brown,1990)。因此,近年来未使用未发芽大麦。
谷物蒸馏厂中的蒸煮
谷物蒸馏厂中用于蒸煮谷物的技术在不断发展,一些蒸馏厂在升级或现代化其工艺时对适应其中一些方法表现出浓厚兴趣。因此,现在苏格兰威士忌的生产有相对广泛的蒸煮选择。这些选择从分批到连续工艺,从压力蒸煮到常压和低温加工,从锤磨谷物到未磨谷物,从小麦到玉米。就可用技术而言,每种选择都有其自身的特点和特定的优缺点。描述谷物威士忌生产蒸煮的出版物包括Pyke(1965),它仍然提供了玉米分批压力蒸煮的权威描述。Rankin(1977)描述了谷物蒸馏厂工艺从更传统的工艺到更现代工艺的演变,类似于今天使用的工艺。Wilkin(1983)介绍了分批和连续工艺,并描述了小麦和玉米的使用。Collicut(2009)主要关注北美谷物威士忌,但也回顾了全球广泛蒸馏厂使用的原材料和技术,包括苏格兰谷物威士忌。Kelsall和Piggott(2009)也描述了一系列蒸煮工艺,其中一些与目前苏格兰威士忌生产中使用的工艺相似。
近年来,人们对利用低温蒸煮系统的兴趣日益增加,至少有一家现代谷物蒸馏厂现已采用该技术。谷物面粉(或未磨谷物)通常在浆料罐中与工艺液混合。根据所使用的工艺和目标原始比重,浆料的浓度可能会有所不同,但通常每公斤谷物含有约2.5升液体(Piggott和Conner,1995;Wilkin,1989)。工艺液通常是水,但也可以包括回收的釜残液(回料)、弱麦汁或从糖化过滤或分离系统中回收的洗糟水。回料是蒸馏过程中釜残液的回收部分,当大部分固体物质已通过离心或筛分去除时(Travis,1998),在某些情况下用作工艺液的补充。尽管回料可能相当酸性,但当正确使用时,它被认为具有重要益处,尤其是在发酵过程中(Travis,1998)。回料可以提供酵母生长必需的营养物质,但过多会导致某些矿物质和离子(如钠和乳酸盐)的供应过剩,这会抑制发酵(Kelsall和Lyons,1999)。现在认为回料是低温蒸煮工艺成功运行的必要条件,并且是加工、水管理、副产品和能量回收系统集成的重要方面。
通常,slurry 罐中的内容物被机械彻底混合,以避免麦芽粉结块,这可能导致提取物损失和未转化淀粉的存在,除了导致酒精产量损失外,还可能在后续过程中引起问题。初始浆料可以在环境温度下进行,但通常在约40°C(或更高)下进行,使用来自该过程的废热。较高的温度有助于麦芽粉的水合和调节,并减少蒸煮所需的能量输入。在某些工艺中,特别是在连续工艺中,添加少量大麦芽作为预麦芽(Collicut,2009)。这样做的目的是利用麦芽中的酶(淀粉酶、蛋白酶和β-葡聚糖酶)部分水解淀粉、蛋白质和胶质(如β-葡聚糖),以降低粘度并促进浆料在该过程中的泵送。
然后将浆料送入蒸煮器,蒸煮器通常是一个圆柱形容器,通常装有搅拌设备(Pyke,1965)。蒸煮过程中的混合对于避免粘连和随后的燃烧(焦糖化)至关重要。然后将蒸汽注入蒸煮器,将浆料加热到所需温度,使淀粉糊化、液化并释放,直到谷物被蒸煮。蒸煮器通常被编程为在固定循环下运行,该循环已针对特定工艺和谷物进行了优化,不同蒸馏厂的蒸煮温度和时间可能会有所不同。实际上,蒸煮温度被编程为升温至最高温度(通常为130至145°C),并在那里仅维持相对较短的时间。对于整粒谷物,需要在高温和高压下更长的时间。一些蒸馏厂可能并行操作多个蒸煮器,以维持足够的半连续生产能力,以支持连续运行的Coffey或专利蒸馏器的蒸馏。
正常的分批蒸煮能耗高,需要相对较长的蒸煮时间,如果工艺控制不当,可能导致过度褐变反应并降低产量。然而,使用分批蒸煮,麦汁更可能是无菌的。分批工艺也更适合使用包括小麦和玉米在内的各种谷物。
总的来说,蒸煮过程代表了糊化、淀粉释放及其热降解为不良产物之间的微妙平衡。如果温度过低,一些淀粉颗粒将保持完整,淀粉不会完全糊化,导致酒精产量损失。另一方面,如果温度过高或淀粉蒸煮时间过长,将发生褐变或美拉德反应。这些反应从降解的淀粉中去除氨基酸、蛋白质和糖,导致酒精产量损失。
表6.6给出了不同蒸馏厂操作的蒸煮温度范围的指示。
| 蒸煮工艺 | 最高温度 |
|---|---|
| 低温 | 68–72°C |
| 常压 | 95–105°C |
| 压力蒸煮(分批) | 125–150°C |
低温连续加工
在20世纪80年代,连续蒸煮被认为在苏格兰谷物威士忌的生产中具有巨大潜力(Wilkin,1989)。然而,由于各种原因,如工艺延迟、能源效率问题和威士忌市场的变化,连续工艺在苏格兰威士忌行业中并未普遍受到青睐,尽管最近兴趣有所增加。在当前的生产计划下,几种现代工艺可被视为半连续的,因为它们仅受发酵过程能力的限制(Palmer,2012)。由于发酵仍然是分批工艺,连续蒸煮特别容易受到下游工艺问题导致的工艺中断的影响。
低温加工有几个优点,因为该系统能耗较低,并减少了粘性细胞壁物质的提取。低温加工的主要好处之一是该系统有可能显著提高酒精产量(Agu等人,2008a),因为底物受工艺条件的破坏较小。然而,现代低温工艺需要与能量回收和副产品流仔细集成,以确保它们以最高效率运行。低温蒸煮的主要缺点是麦汁可能不完全无菌,因此必须仔细管理该系统,以避免微生物感染的积累,这可能在发酵阶段引起问题。
目前,只有一家谷物蒸馏厂正在使用真正的低温(68至72°C)蒸煮工艺,但它仍然依赖很大比例的高温(>140°C)/压力生产来支持整体生产水平。在一定水平上维持高温工艺被认为是蒸馏厂能量平衡的关键组成部分,它提供了必要的备份,以确保维持生产效率。
采用低温蒸煮/糖化工艺需要对传统的谷物蒸馏厂工艺进行一些重要改变,特别是引入回料,现在回料被视为这种工艺的必要组成部分。没有回料,很难从低温工艺中持续获得良好的酒精产量。这主要是因为当回料返回该过程时,它可以提供额外水平的可溶性氮和FAN来支持发酵,这可能比正常情况更慢。此外,向每个发酵罐中添加一定比例的高温蒸煮糖化液也提供了一些好处,因为高温工艺也有助于麦汁中的可溶性氮。
在现代低温连续蒸煮中,小麦被锤式研磨,麦芽粉通过2.5毫米的筛网筛分,得到一种面粉,与水混合时容易水合。小麦粉和小比例的麦芽(预麦芽)在45至55°C下与工艺液制成 slurry,并在前往糖化/转化容器的途中加热至约68至72°C,在那里与正常糖化温度(63至64°C)的麦芽浆料混合。多个蒸煮和转化容器的并行使用允许维持连续的生产流。糖化/转化后,含谷物的麦汁被冷却并添加到发酵罐中。
蒸馏后,废洗液被离心以去除剩余的固体,清澈的离心液作为回料返回该过程。密切监测回料以确保pH合适(约pH 4),并在下次糖化前添加到谷物浆料中。回料通常占低温蒸煮工艺液的约40至50%。
低温和高温工艺相结合的关键方面是热回收系统在该过程中的集成方式,以及优化方式以支持蒸馏厂的能量平衡,从而减少外部输入并最小化碳足迹。
美拉德反应
美拉德或褐变反应是一系列高度复杂的反应,发生在高温条件下糖与氨基酸或蛋白质之间,产生一系列深色色素产物。这些反应在文献中已被广泛综述(Briggs等人,2004;Hough等人,1982;O’Brien等人,1998),本章不试图详细涵盖该主题;然而,图6.14给出了所涉及过程的复杂性的概念。
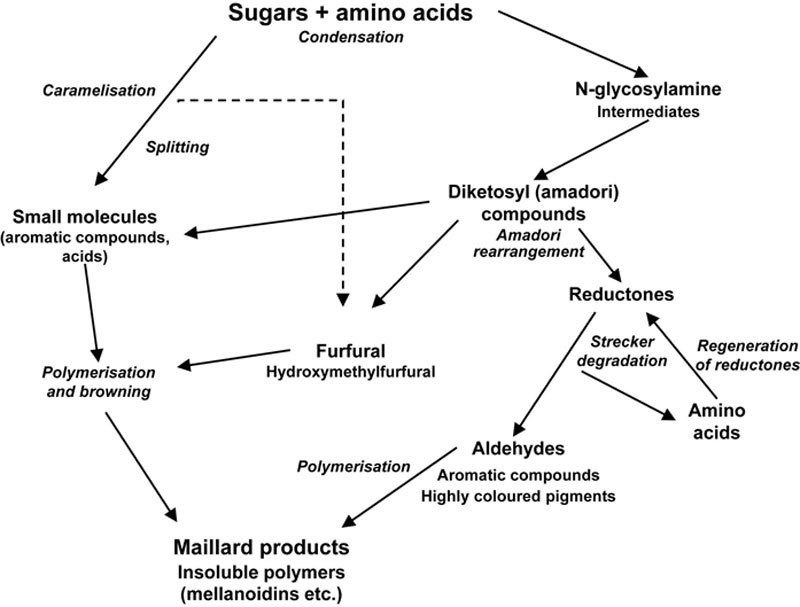
图6.14 美拉德(褐变)反应涉及的过程总结。改编自Adrian, J.等人(1988)。
Mlotkiewicz(1998)描述了美拉德反应的主要阶段。最初,还原糖与氨基酸结合形成产物(Amidori或Heynes重排产物),这些产物通过一系列复杂的反应降解为大量风味中间体和其他风味活性化合物。关键路线之一是Strecker降解,其中氨基酸与称为还原酮的二羰基化合物反应形成最终也转化为棕色色素聚合物材料的产物。美拉德反应的最终产物是含有两到四个连接环的低分子量有色化合物和分子量高得多的类黑精的混合物。此外,还产生大量其他风味和香气活性产物,如呋喃、吡咯和环状硫化合物。美拉德产物的形成通过升高温度、加热时间和pH(特别是pH 7以上)而增强。
蒸煮过程中美拉德反应的发生很重要,因为它们导致可发酵碳水化合物和氨基酸的摄取和降解,并可能对酒精产量产生重大影响(图6.15)。它们还对下游加工和可能导致副产品问题产生影响。
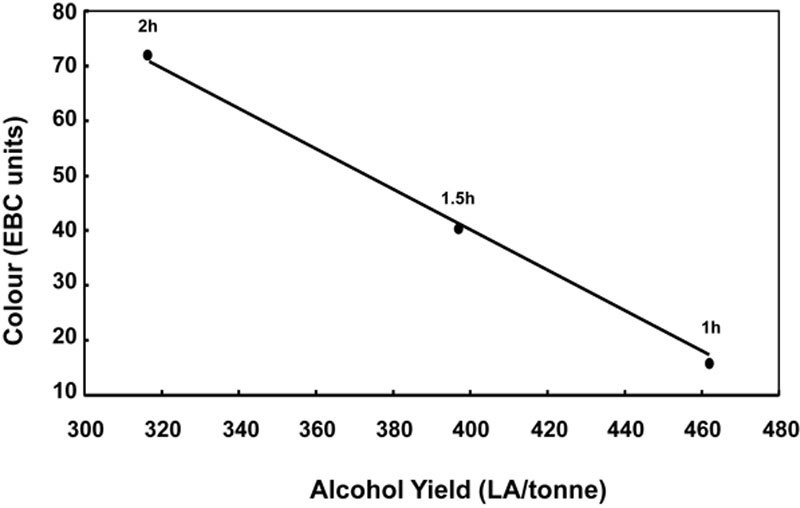
图6.15 实验室数据显示小麦在延长时间(145°C下1、1.5和2小时)下麦汁颜色与酒精产量的反比关系(苏格兰威士忌研究所数据)。
最佳蒸煮时间和温度在很大程度上取决于所使用的谷物和所采用的工艺。玉米通常比小麦需要更高的温度和/或更长的蒸煮时间。研磨程度也很重要。精细研磨的谷物比未研磨的谷物需要更短的蒸煮时间,未研磨的谷物可能需要长达2小时(Brown,1990)。
只要使用更长的蒸煮时间是经济的,未研磨谷物的压力蒸煮可以既高效又具有成本效益(Bathgate,1989)。此外,当排污时释放压力,谷物胚乳在被输送到转化阶段时会被彻底分解。有人认为整粒谷物加工阶段不太容易出现过度蒸煮或褐变的问题。无壳谷物如小麦和玉米更适合整粒蒸煮,因为它们在蒸煮后分解得更彻底(Walker,1986)。
排污和回生
当煮熟的谷物浆料从压力蒸煮器中排出时,通常排入闪蒸冷却容器或膨胀罐,压力迅速降低。这被称为排污,其作用是机械地从谷物基质中释放任何剩余的紧密结合的淀粉(爆米花效应)。当排出煮熟的整粒谷物时,蒸煮器转移相关的管道有助于确保谷物的分解(Walker,1986)。
排污是蒸煮过程的关键部分,通常与快速但仔细控制的冷却相关。不良的温度控制将导致回生(凝沉)的严重问题,这将导致煮熟的浆料形成抵抗酶分解的凝胶(MacGregor和Fincher,1993),并导致与粘度(Swinkels,1985)、过滤性和酒精产量(Jameson等人,2001)相关的后续加工问题。
回生被定义为从分散的无定形状态转变为不溶性结晶状态(Swinkels,1985),当加热的糊化淀粉在冷却时开始重新缔合(Atwell等人,1988),导致凝胶形成和沉淀时发生。回生过程非常复杂(Swinkels,1985),但被认为主要受淀粉中直链淀粉的相对量影响(Sasaki等人,2000)。回生涉及的其他重要因素是蒸煮条件、淀粉浓度、冷却程序和pH。小麦和玉米淀粉各含有26至28%的直链淀粉,都容易回生。蜡质玉米实际上全是支链淀粉,回生的可能性要小得多。
直链淀粉链的长度被认为对回生过程中发生的过程有重大影响。这会影响诸如形成沉淀或凝胶的倾向和凝胶强度等参数。较长的链长(>1100个单位)由于相邻链的排列和交联形成有序结构,显示出更强的凝胶形成趋势(Hoover,1995)。
通常,回生是由于相邻直链淀粉分子链之间的氢键结合而发生的,这些链不可逆地结合在一起形成聚集体。这种交联可能涉及单个直链淀粉链内的多个区域,导致形成大分子网络(Hoover,1995)。聚集的物质将液体截留在部分缔合的淀粉分子网络中,导致凝胶的形成(Swinkels,1985)。回生速率在pH 5和pH 7之间最高。pH 10以上不发生回生,pH 2以下仅缓慢进行。回生的直链淀粉不易被α-淀粉酶降解(Miles等人,1985a)。因此,当淀粉回生时,极难再次溶解。直链淀粉的回生被认为是不可逆的,即使在高温(高于100°C)下也是如此(Miles等人,1985b)。图6.16说明了回生的主要特征。
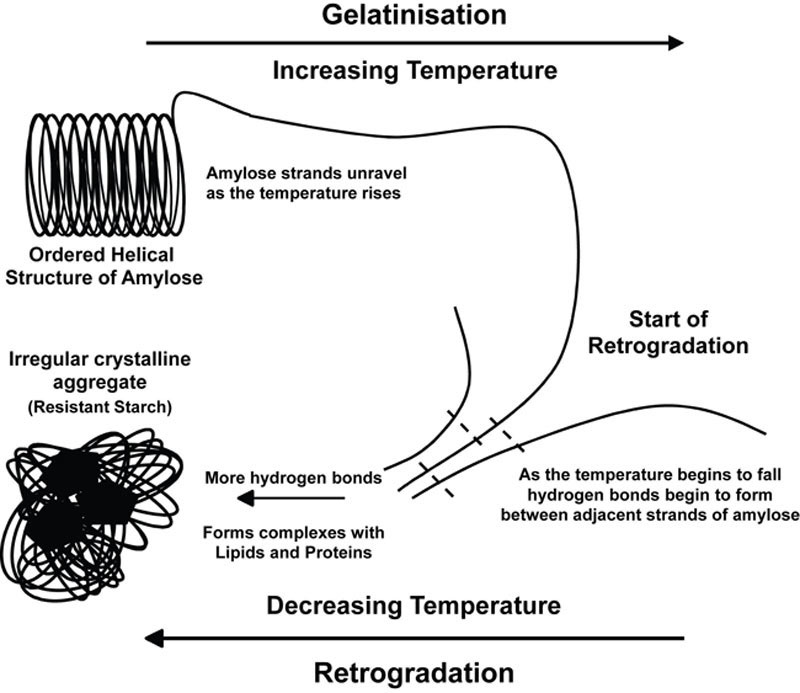
图6.16 淀粉的回生。
支链淀粉比直链淀粉更不容易回生,这种聚合物的存在被认为是对该过程的调节影响(Swinkels,1985)。然而,在极端条件下,如高淀粉浓度和极低温度,支链淀粉也会发生回生,但这在一定程度上是可逆的(Miles等人,1985b)。玉米支链淀粉比大麦或小麦更容易回生,并且回生更快。这归因于玉米支链淀粉的更高结晶度和更大比例的DP 15至20的链。小麦支链淀粉比大麦支链淀粉更不容易回生(Hoover,1995)。
正常回生在淀粉冷却时发生,但也可能在高温(75至95°C)下储存淀粉溶液时发生。这表现为规则尺寸颗粒的沉淀。这种现象似乎与形成与直链淀粉复合的脂质或脂肪酸物质的存在有关。这些复合物在95°C以上不形成(Swinkels,1985)。Jameson等人(2001)观察到,在糖化前将煮熟的玉米或小麦在谷物蒸馏厂中保持在高达100°C的温度下,会导致抗性淀粉的形成,这可能导致蒸馏过程中的后续问题。
在排污过程中,温度迅速降至约70°C,这非常接近麦芽的正常投料温度。这允许以这样的方式添加麦芽,即麦芽酶在回生发生之前开始快速水解煮熟的淀粉。这代表了一种非常微妙的平衡,该过程需要仔细控制。如果麦芽添加太晚或投料温度太低,煮熟的淀粉将开始回生并变得不可接近。如果麦芽添加太早,投料温度将太高,麦芽酶将被破坏,也会导致产量损失。
蒸煮中的问题
蒸煮过程中存在几个主要问题来源。当蒸煮时间太短或没有足够的热量使淀粉正确糊化时,会发生蒸煮不足。这会导致酒精产量的显著损失,因为未糊化的淀粉不易被酶水解。这在连续加工中可能是一个特殊问题,但也可能与谷物质量的变化有关,如小麦氮含量和研磨性能。当浆料过度蒸煮时,会发生过度褐变(美拉德)反应,这会从麦汁中去除可发酵底物和蛋白质物质,导致酒精产量损失。过度蒸煮还会因煮熟的浆料焦糖化而导致粘连和燃烧的物理问题。与小麦相关的更高水平的细胞壁物质和胶质(如β-葡聚糖和阿拉伯木聚糖)也会在蒸煮过程中导致粘度问题,但这些往往具有更严重的下游影响,特别是对蒸馏后副产品的回收。如果蒸煮和排污过程没有仔细控制,回生可能是一个问题。当淀粉回生时,它变得不溶且无法被酶水解,并且将无法产生可发酵糖,导致酒精产量的显著损失。
转化
转化原理
当蒸煮器卸料时,煮熟的浆料随后被添加到已保持在特定温度(通常约为40°C,但有时更高且更接近糖化温度)的麦芽浆料中。在某些情况下,煮熟的谷物在冷却至合适的投料温度后直接排入含有麦芽的容器(滴罐);在其他情况下,麦芽浆料被添加到煮熟的谷物中,要么直接进入工艺流(连续工艺),要么进入转化容器。所使用的实际程序取决于各个工艺。这些方法各有优缺点。选择主要由现有技术和各个工艺的经济性决定。
转化的主要功能是将糊化淀粉分解为可发酵糖和小糊精(淀粉水解)。将蛋白质降解为氨基酸和低分子量、富含氮的片段也至关重要,这些是发酵过程中为酵母提供营养所必需的。由于苏格兰谷物威士忌的生产中不允许添加添加剂,因此这两个过程都必须完全通过麦芽中的内源酶来完成。这与中性烈酒的生产形成对比,后者允许使用添加的商业生产食品级酶。
用于转化的麦芽通常是商业生产的高酶麦芽,已发芽并仔细干燥(烘烤)以产生高水平的α-和β-淀粉酶(DU/DP)。一些绿麦芽(未烘烤的)仍在使用,但在大多数谷物蒸馏厂中已被烘烤麦芽取代。绿麦芽的生产成本通常比烘烤麦芽低,并且有可能以较低的剂量(麦芽掺入率)使用;然而,它的保质期比干麦芽短,运输成本也更高(Walker,1986)。
在糖化之前,通常使用锤式磨机将麦芽研磨成细粉,然后用工艺液(通常是水)制成 slurry。在与煮熟的谷物浆料混合之前,将该浆料在合适的温度(约40°C)下调节短时间(20至30分钟)。重要的是,slurry 罐中的停留时间应保持最短,以避免麦芽浆料中微生物感染水平的积累,因为这可能影响糖化效率和发酵性能。如果使用绿麦芽,通常在与煮熟的谷物混合之前将其湿磨成 slurry。典型地,苏格兰威士忌谷物蒸馏厂中使用的大麦芽量(麦芽掺入率)约为总谷物量的10%(以干重计),尽管不同蒸馏厂可能有所不同,在某些情况下可能低于10%或高达15%。
在蒸煮器卸料后必须尽快添加麦芽,以便麦芽中的酶(主要是α-淀粉酶)可以在淀粉开始回生前开始降解溶解的淀粉,降低粘度。如上所述,煮熟的淀粉的长时间储存将导致回生和抗性淀粉的形成,这不会被酶有效降解。
在许多情况下,麦芽浆料和煮熟的谷物浆料在糖化桶或其他转化容器中混合,并在糖化温度(62至65°C)下保持长达30分钟,以将淀粉转化为可发酵糖,主要是麦芽糖。在连续管式转化器中,由于增加的热传递和麦芽酶与谷物浆料之间更紧密的接触,停留时间可以大大缩短。Robson(2001)描述了谷物蒸馏厂中的连续转化容器,其中平均停留时间约为20分钟。转化时间应足以将淀粉完全转化为可发酵糖。
与转化相关的主要问题是淀粉未完全转化为可发酵糖,这表现为麦汁中高水平的低聚糖和糊精。这可能是由于转化过程中温度控制不佳、转化时间不足或由于麦芽掺入率过低或麦芽质量差导致麦芽中酶不足的结果。此外,pH水平可能过低,无法实现最佳酶性能(例如,由于使用了过高比例的回料)。在转化过程中,糖化pH水平通常约为5.0至5.5,这有利于α-和β-淀粉酶的活性。谷物蒸馏与酿造的区别之一是麦汁在发酵前不煮沸。这允许酶在发酵过程中保持活性。在发酵的早期阶段,pH降至4.2至4.4,这将导致脱支酶极限糊精酶的活性形式的释放和作用(Bryce等人,2004;Walker等人,2001)。麦芽酶仍然活跃,并将在发酵过程中继续缓慢降解糊精(Bringhurst等人,2001),但如果转化过程没有有效进行,它们将无法降解任何大量剩余的未降解淀粉。
麦汁分离
传统上,在谷物蒸馏厂中,转化后在糖化桶中分离麦汁,并用温度逐渐升高的液体多次喷洒,以提供清澈、过滤的麦汁用于发酵,这与麦芽蒸馏厂的方式大致相同(Rankin,1977)。然而,就现代谷物蒸馏厂的生产需求而言,该过程复杂且耗时,在现代谷物蒸馏厂中,麦汁分离已在很大程度上被淘汰。在用麦芽转化后,通常在冷却和接种酵母后将整个糖化液直接转移到发酵罐。这允许使用比其他情况更高的原始比重(高达1085°,或21°柏拉图)。
然而,使用未过滤的麦汁可能导致蒸馏过程中蒸馏器结垢,并可能产生严重的下游影响,特别是对用于收集副产品的蒸发器的高效运行。蒸发器的问题可能导致大量工艺延迟,这对整个谷物蒸馏厂工艺的效率产生严重影响。这些问题在一定程度上可以通过蒸馏后从废洗液中去除固体物质(如通过离心)来缓解。
在一些谷物蒸馏厂中,由于加工限制,认为有必要在将麦汁泵送到发酵罐之前进行某种分离过程。使用麦汁分离过程的主要优点是将主要为液体的麦汁泵送到发酵容器,这将在随后的蒸馏和副产品加工过程中引起较少的问题。然而,过滤过程本身可能导致生产周期的延迟,这可能对工厂效率产生严重影响(Jameson等人,2001)。在废谷物中损失残留淀粉的可能性也更大,这可能导致酒精产量的显著损失。此外,由于糖化过程中仅溶解约10至15%的总蛋白质(Boivin和Martel,1991),大部分剩余的未水解蛋白质仍留在废谷物中。这意味着可能存在游离氨基氮的潜在短缺,无法维持足够水平的酵母发酵。
苏格兰威士忌谷物蒸馏厂采用了几种不同的分离方法。最初,使用过滤类型的过滤系统过滤麦汁(Pyke,1965),但这些早已被其他更适应或多或少连续操作的过滤系统所取代。在这种系统中,糖化液通过一系列过滤器或筛子(水力筛)过滤(Robson,2002),并喷洒谷物以去除可溶性物质。第一和第二麦汁被泵送到发酵罐,回收的洗糟水(弱麦汁)被循环回该过程。在很大程度上,这些操作方式与传统麦芽蒸馏厂的麦汁分离过程类似,尽管使用的设备完全不同。麦汁分离的要求主要由特定工艺的效率和经济性以及各个公司的技术经验决定。
总的来说,谷物蒸馏厂工艺比麦芽蒸馏厂的工艺复杂得多,在提高工艺效率和更好地管理能源和水资源方面有更大的技术创新机会,这也是蒸馏厂可持续发展和环境目标的重要特征。
作为原材料的水
水是关键原材料之一,在第17章中单独讨论。
未来趋势
麦芽蒸馏厂的工艺往往比谷物蒸馏厂更传统且适应性更弱,未来创新的主要领域可能集中在幕后技术。改进的过程控制将提供更高效、集成的能源利用和热回收系统,并根据行业气候变化和可持续发展目标减少用水量和环境排放。成功的合作项目已将利益相关者群体聚集在一起,包括植物育种者、农学家、学者、麦芽制造商、啤酒酿造商和蒸馏商,以密切研究改善蒸馏厂性能的潜在方法,同时保持他们对可持续发展的承诺。
一个看起来非常有前途的领域是开发更适合麦芽蒸馏厂加工的现代高产大麦品种。这主要归功于植物育种者用于识别有前途的新材料的遗传工具的开发和改进,这将有助于加速开发新大麦品种的经典(非转基因)育种方法。我们已经有了糖苷腈(EPH)的可靠遗传标记(Swanston等人,1999),但其他具有经济重要性的农艺和最终用户性状的标记正在开发中,这将有助于满足蒸馏商、麦芽制造商和啤酒酿造商的未来需求(Bringhurst等人,2012b)。类似的方法也被用于改善我们对小麦遗传学的理解,可应用于苏格兰谷物威士忌生产和生物乙醇生产(Bringhurst等人,2012b;Sylvester-Bradley等人,2010)。
从技术角度来看,在苏格兰威士忌的法律定义限制内,谷物蒸馏厂工艺对技术变化的适应性更强,比麦芽蒸馏厂更容易进行技术创新。这种灵活性允许使用更广泛的潜在原材料,这主要由市场力量驱动。此外,谷物蒸馏的经济性可以支持从谷物威士忌向其他中性烈酒的多样化,如伏特加或杜松子酒,以提供尽可能广泛的产品系列。本质上,生产这些产品的技术与谷物威士忌的技术相同,可能除了蒸馏阶段,但生产不受苏格兰威士忌法律定义的限制。此外,对于中性烈酒,还可以使用商业淀粉降解酶代替相对昂贵的麦芽,用于伏特加和杜松子酒等中性烈酒衍生的产品。然而,在生产多种产品的蒸馏厂中,应将苏格兰威士忌生产流与其他烈酒的生产流严格分离,以避免苏格兰威士忌工艺受到污染,从而保持苏格兰谷物威士忌的完整性。
那么,苏格兰谷物威士忌未来生产的可能发展是什么?目前,所使用的技术在很大程度上取决于现有工艺的范围,以及根据修改现有工艺的相对资本成本和采用新技术的经济性如何发展,以响应定义需求产品的市场压力以及可用的原材料。
谷物威士忌生产的主要选择原材料是软冬小麦,并且可能会继续如此。然而,有人担心,由于未来环境威胁(如收获条件差或欧盟管理干预的法规变化)导致的小麦市场近期变化,可能会影响苏格兰威士忌生产商使用的小麦供应,这可能会削弱小麦相对于玉米的经济优势。这就是为什么谷物蒸馏厂在可能的情况下可能希望保留加工玉米以及潜在其他谷物的能力的原因之一。
随着工艺技术的不断发展,苏格兰威士忌生产商现在可以获得更广泛的工艺选择,无论是在传统的分批和连续蒸煮工艺方面,还是在引入高效蒸煮系统(如蒸汽喷射蒸煮器)方面,这些系统可以在更高温度(160°C)下运行,并且还可以轻松与现代能源和水回收系统集成,这些系统可以适应分批和连续蒸煮工艺(Collicut,2009)。
由于小麦的糊化温度相对于玉米较低(Bathgate,1989),因此可以在比玉米更低的温度下加工小麦,并且已经表明这有可能提供更高的酒精产量和降低废洗液粘度(Agu等人,2008a)。现在苏格兰谷物威士忌生产商对更广泛地完善和应用该技术有了更广泛的兴趣。现代低温工艺可以结合精细研磨和70至85°C范围内的温度,使小麦淀粉充分糊化,以提供高酒精产量和生产吞吐量。
Wilkin(1989)回顾了一些无蒸煮或冷蒸煮工艺。早在1980年至1984年,这些工艺就以不同程度的成功被使用。在这些工艺中,谷物和块茎淀粉被用于在低至55°C的温度下产生大量酒精产量。然而,原材料需要被超细研磨,这消耗了通过降低蒸煮温度节省的大量能源。还遇到了淀粉颗粒不完全释放和糖化的问题,这只能通过添加外源酶(如蛋白酶和半纤维素酶)来解决,因此不能用于当前定义的苏格兰威士忌的制造。
仔细选择合适的原材料是使冷蒸煮或低温工艺更有效工作的关键方面。Agu等人(2008a)强调了对一系列不同小麦品种的实验室工作,证实了谷物蒸馏厂中低温加工的潜力。随着专门选择的小麦和大麦新品种的出现,现在在未来商业上使用这种工艺是可行的(Agu等人,2008b)。
苏格兰谷物威士忌的一个明显方向是修改工艺以使其真正连续(Rankin,1990)。Whitby(1995)预测,从长远来看,蒸馏厂最终将通过更有效地利用原材料和最少使用能源与酒精的最大生产完全集成,很明显,当前的趋势是各个蒸馏公司稳步朝着这个方向发展。
在这个阶段,很难说苏格兰威士忌行业是否准备好完全朝着全作物利用的方向发展,如Petersen和Munck(1993)以及Bekers等人(1997)所描述的,其中蒸馏厂生产过程是封闭生物技术系统或生物精炼厂的一部分(Audsley和Sells,1997;Lyons,1999),允许原材料的完全利用,以生产广泛的可销售副产品以及乙醇(威士忌)。然而,最终,蒸馏的未来方向可能是作为谷物加工者,而不是专门的酒精生产者(Lyons,1999)。其中一些目标在当时主要是雄心勃勃的,但现在已成为解决该行业长期可持续发展目标的当前举措的核心。
采用部分集成的副产品处理系统,如图6.17所示,表明苏格兰威士忌行业在这个方向上已经走了多远。现在,该行业的一个重要目标是完善整个蒸馏厂工艺的组织方式,以结合现代能源回收系统,有效和可持续地利用原材料和副产品,使他们能够通过采用可再生能源和循环水来实现环境和可持续发展目标并减少碳足迹。现在运行的应用包括使用生物质发电、改善水管理、使用好氧和厌氧消化和膜生物过滤,以及改进的热回收系统(Jappy,2010)。
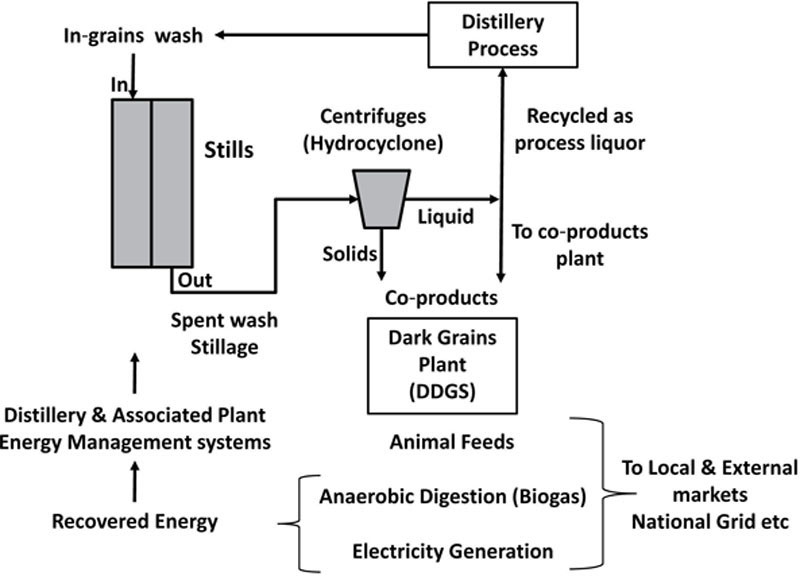
图6.17 典型谷物蒸馏厂中的集成副产品处理系统。
苏格兰谷物威士忌生产的潜在未来技术发展在很大程度上已经在其他领域到位,目前正在用于为从酿造到制药再到燃料酒精的其他行业生产各种其他谷物、发酵和蒸馏产品。然而,具有良好蒸馏厂加工和稳健农艺特性的新大麦和小麦品种的研发是关键优先事项。
将谷物加工成苏格兰谷物威士忌的新技术的采用仍然取决于市场压力和苏格兰威士忌行业面临的其他未来经济因素。苏格兰威士忌行业面临的挑战将继续是其在保持市场地位的同时利用新技术的能力,但又不失去其产品的独特品质。
参考文献
-
Adrian J, Legrand G, Frangne R. Dictionary of Food and Nutrition. Chichester: Ellis Horwood; 1988:pp. 120–121.
-
Agu RC, Palmer GH. α-Glucosidase activity in sorghum and barley. Journal of the Institute of Brewing. 1997;103:25–29.
-
Agu RC, Bringhurst TA, Brosnan JM. Production of grain whisky and ethanol from wheat, maize and other cereals. Journal of the Institute of Brewing. 2006;112(4):314–323.
-
Agu RC, Bringhurst TA, Brosnan JM, Jack FR. Effect of process conditions on alcohol yield of wheat, maize and other cereals. Journal of the Institute of Brewing. 2008;114(1):39–44.
-
Agu RC, Swanston JS, Bringhurst TA, Brosnan JM, Jack FR, Smith PL. The influence of nitrogen content and corn size on the quality of distilling wheat cultivars. In: Bryce JH, Piggott JR, Stewart GG, eds. Distilled Spirits: Production, Technology and Innovation. Nottingham, U.K.: Nottingham University Press; 2008:67–74.
-
Agu RC, Bringhurst TA, Brosnan JM. Effect of batch-to-batch variation on the quality of laboratory and commercially malted Oxbridge barley. Journal of the Institute of Brewing. 2012;118(1):49–56.
-
Atwell WA, Hood LF, Lineback DR, Varriano Marston E, Zobel HF. The terminology and methodology associated with basic starch phenomena. Cereal Foods World. 1988;33:306–311.
-
Audsley E, Sells J. Determining the profitability of a whole crop biorefinery. In: Campbell GM, Webb C, McKee SL, eds. Cereals: Novel Uses and Processes. New York: Plenum Press; 1997:191–203.
-
Badr A, Muller K, Schafer-Pregl R, El Rabey H, Effgen S, Ibrahim HH. On the origin and domestication history of barley (Hordeum vulgare). Molecular Biology and Evolution. 2000;17(4):449–510.
-
Bamforth CW, Quain DE. Enzymes in brewing and distilling. In: Palmer GH, ed. Cereal Science and Technology. Aberdeen, Scotland: Aberdeen University Press; 1989:326–366.
-
Barnes PJ. Wheat in milling and baking. In: Palmer GH, ed. Cereal Science and Technology. Aberdeen: Aberdeen University Press; 1989:367–412.
-
Bathgate GN. Cereals in Scotch whisky production. In: Palmer GH, ed. Cereal Science and Technology. Aberdeen, Scotland: Aberdeen University Press; 1989:243–278.
-
Bathgate GN. The recipe for Scotch whisky. In: Beach RHB, ed. Brewing Room Book 1998-2000. Bury St. Edmunds, U.K.: Pauls Malt, Ltd; 1998:81–84.
-
Bathgate GN. History of the development of whisky distillation. In: Russell I, ed. Whisky: Technology, Production and Marketing. London: Academic Press; 2003:2–24.
-
Bathgate GN, Bringhurst TA. Letter to the Editor: Update on knowledge regarding starch structure and degradation by malt enzymes (DP/DU and Limit dextrinase). Journal of the Institute of Brewing. 2011;117(1):33–38.
-
Bathgate GN, Cook R. Malting of barley for Scotch whisky production. In: Piggott JR, Sharp R, Duncan REB, eds. The Science and Technology of Whiskies. Harlow, U.K.: Longman Scientific & Technical; 1989:19–63.
-
Bathgate GN, Palmer GH. The in vivo and in vitro degradation of barley and malt starch granules. Journal of the Institute of Brewing. 1973;79:402–406.
-
Bathgate GN, Clapperton JF, Palmer GH. The significance of small starch granules. European Brewery Convention Proceedings. 1973;14:183–196.
-
Bekers M, Laukevics J, Vedernikovs N, Ruklisha M, Savenkova L. A closed biotechnological system for the manufacture of non-food products from cereals. In: Campbell GM, Webb C, McKee SL, eds. Cereals: Novel Uses and Processes. New York: Plenum Press; 1997:169–176.
-
Boivin P, Martel C. Proteolysis during malting. Ferment. 1991;4:182–186.
-
Briggs, DE., Hough, JS., Stevens, R., and Young, TW., Eds. 1981. Malting and Brewing Science. Vol. 1. Malt and Sweet Wort, 2nd ed. Chapman & Hall, London.
-
Briggs DE, Boulton CA, Brookes PA, Stevens R. Brewing Science and Practice. Cambridge, U.K: Woodhead Publishing; 2004.
-
Bringhurst TA, Broadhead AL, Brosnan JM, Pearson SY, Walker JW. The identification and behaviour of branched dextrins in the production of Scotch whisky. Journal of the Institute of Brewing. 2001;107:137–149.
-
Bringhurst TA, Brosnan JM, Fotheringham AL. Grain whisky: raw materials and processing. In: Russell I, ed. Whisky: Technology, Production and Marketing. London: Academic Press; 2003:77–115.
-
Bringhurst TA, Agu RC, Brosnan JM, Fotheringham AL. Wheat for Scotch whisky production: broadening the horizon. In: Bryce JH, Piggott JR, Stewart GG, eds. Distilled Spirits: Production, Technology and Innovation. Nottingham, U.K.: Nottingham University Press; 2008:51–66.
-
Bringhurst TA, Agu RC, Brosnan JM. Creating better cereal varieties for the sustainability of the distilling industry. In: Walker GM, Goodall I, Fotheringham R, Murray D, eds. Distilled Spirits: Science and Sustainability. Nottingham, U.K.: Nottingham University Press; 2012:77–86.
-
Bringhurst TA, Brosnan JM, Thomas WTB. New approach to barley breeding. AGOUEB—The Association Genetics of UK Elite Barley Project. Brewer and Distiller International. 2012;8(1):25–28.
-
Brosnan JM, Makari S, Paterson L, Cochrane MP. What makes a good grain distillery wheat? In: Campbell I, ed. Proceedings of the Fifth Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1999:225–228.
-
Brosnan JM, Bringhurst TA, Agu RC. Growing sustainability in the wheat supply chain. In: Walker GM, Hughes PS, eds. Distilled Spirits: New Horizons: Energy, Environment and Enlightenment. Nottingham, U.K.: Nottingham University Press; 2010:27–32.
-
Brown JH. Assessment of wheat for grain distilling. In: Campbell I, ed. Proceedings of the Third Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1990:34–47.
-
Bryce JH, Stewart GG. Distilled Spirits: Tradition and Innovation. Nottingham, U.K: Nottingham University Press; 2004.
-
Bryce JH, McCafferty CA, Cooper CS, Brosnan JM. Optimising the fermentability of wort in a distillery: the role of limit dextrinase. In: Bryce JH, Stewart GG, eds. Distilled Spirits: Tradition and Innovation. Nottingham, U.K.: Nottingham University Press; 2004:69–78.
-
Bryce JH, Piggott JR, Stewart GG, eds. Distilled Spirits: Production, Technology and Innovation. Nottingham, U.K: Nottingham University Press; 2008.
-
Bryce JH, Goodfellow V, Agu RC, Brosnan JM, Bringhurst TA, Jack FR. Effect of different steeping conditions on endosperm modification and quality of distilling malt. Journal of the Institute of Brewing. 2010;116(2):125–133.
-
Buglass AJ. Handbook of Alcoholic Beverages. Chichester: John Wiley & Sons; 2011.
-
Bushuk W. Wheat: chemistry. Cereal Foods World. 1986;31(3):218–226.
-
Cochrane MP. Seed carbohydrates. In: Black M, Bewley JD, eds. Seed Technology and Its Biological Basis. Sheffield, U.K.: Sheffield Academic Press; 2000:85–120.
-
Collicut H. Whisky: grain mashing and fermentation. In: Ingledew WM, Kelsall DR, Austin GD, Kluhspies C, eds. The Alcohol Textbook. 5th ed. Nottingham, U.K.: Nottingham University Press; 2009:413–430.
-
Cook R. The formation of ethyl carbamate in Scotch whisky. In: Campbell I, ed. Proceedings of the Third Aviemore Conference on Malting Brewing and Distilling. London: Institute of Brewing; 1990:237–243.
-
DEFRA., 2012. Agriculture in the United Kingdom, 2011, pp. 29–34. Department for Environment, Food and Rural Affairs, London (http://www.defra.gov.uk/statistics/foodfarm/cross-cutting/auk/).
-
Dengate HN, Swelling, pasting, and gelling of wheat starch. Pomeranz Y, ed. Advances in Cereal Science and Technology, VI. St. Paul, MN: American Association of Cereal Chemists; 1984:49–82.
-
Dolan TCS. Some aspects of the impact of brewing science on Scotch Malt whisky production. Journal of the Institute of Brewing. 1976;82:84–86.
-
Dolan TCS. Malt whiskies: raw materials and processing. In: Russell I, ed. Whisky: Technology, Production and Marketing. London: Academic Press; 2003:27–74.
-
European Brewery Convention Analytica-EBC. Nürnberg, Germany: Fachverlag Hans Carl; 2010.
-
European Parliament and Council of the European Union. (2008). Regulation (EC) No. 110/2008 of the European Parliament and of the Council of 15 January 2008 on the definition, description, presentation, labelling and the protection of geographical indications of spirit drinks and repealing Council Regulation (EEC) No. 1576/89. Official Journal of the European Union, February 13, pp. 16–54.
-
Evers AD, Stevens DJ, Starch damage. Pomeranz Y, ed. Advances in Cereal Science and Technology, VII. St. Paul, MN: American Association of Cereal Chemists; 1985:321–349.
-
FAOSTAT. (2012). Food and Agriculture Organization of the United Nations (FAOSTAT) data, www.fao.org.
-
Fincher GB, Stone BA. Physiology and biochemistry of germination in barley. In: MacGregor AW, Bhatty RS, eds. Barley: Chemistry and Technology. St. Paul, MN: American Association of Cereal Chemists; 1993:247–295.
-
Fredriksson H, Silverio J, Andersson R, Eliason A-C, Åman P. The influence of amylose and amylopectin characteristics on gelatinisation and retrogradation properties of different starches. Carbohydrate Polymers. 1998;35:119–134.
-
French D. Organisation of starch granules. In: Whistler RL, BeMiller JN, Paschall EF, eds. Starch: Chemistry and Technology. 2nd ed. London: Academic Press; 1984:183–247.
-
Gray AS. The Scotch Whisky Industry Review. 35th ed. Edinburgh: Sutherlands; 2012.
-
Harrison BM. Impact of peat source on the flavour of Scotch malt whisky. In: Walker GM, Goodall I, Fotheringham R, Murray D, eds. Distilled Spirits: Science and Sustainability. Nottingham, U.K.: Nottingham University Press; 2012:19–26.
-
Harrison BM, Ellis J, Broadhurst D, Reid KJG, Goodacre R, Priest FG. Differentiation of peats used in the preparation of malt for Scotch whisky production using Fourier transform infrared spectroscopy. Journal of the Institute of Brewing. 2006;112(4):333–339.
-
Hesketh-Laird J, Hutcheon G, Rae D. Sustainable Scotch: will science deliver the industry’s sustainability strategy or will the strategy deliver the science. In: Walker GM, Goodall I, Fotheringham R, Murray D, eds. Distilled Spirits: Science and Sustainability. Nottingham, U.K.: Nottingham University Press; 2012:323–329.
-
HGCA HGCA Recommended Lists 2012/13 for Cereals and Oilseeds. Kenilworth: Home Grown Cereals Authority, Agriculture and Horticulture Development Board; 2012.
-
Hoover R. Starch retrogradation. Food Reviews International. 1995;11:331–346.
-
Hough, JS, Briggs, DE, Stevens, R, and Young, TW (1982). Malting and Brewing Science. Vol. 2. Hopped Wort and Beer, 2nd ed. Chapman & Hall, London.
-
Hume JR, Moss MS. The Making of Scotch Whisky. 2nd ed. Edinburgh: Canongate Books; 2000.
-
Ingledew WM, Kelsall DR, Austin GD, Kluhspies C, eds. The Alcohol Textbook. 5th ed. Nottingham, U.K: Nottingham University Press; 2009.
-
IOB., 1997. IOB Methods of Analysis. Vol. 1. Analytical, Methods. Institute of Brewing, London.
-
Jacques KA, Lyons TP, Kelsall DR, eds. The Alcohol Textbook. 4th ed. Nottingham, U.K: Nottingham University Press; 2003.
-
Jameson RPM, Palmer GH, Spouge J, Bryce JH. Resistant starch formation in the distillery. Journal of the Institute of Brewing. 2001;107:3–10.
-
Jane J, Chen YY, McPherson AE, Wong KS, Radosavljievic M, Kasemsuwan T. Effects of amylopectin branch chain length and amylose content on the gelatinization and pasting properties of starch. Cereal Chemistry. 1999;76:629–637.
-
Jappy, M., 2010. New build distilleries—challenges of sustainability. In: Distilled Spirits. Vol. 3. New Horizons: Energy, Environment and Enlightenment (G.M. Walker and P.S. Hughes, Eds.), pp. 105–110. Nottingham University Press, Nottingham, U.K.
-
Jones BL, Marinac L. The effect of mashing on malt endoproteolytic activities. Journal of Agriculture and Food Chemistry. 2002;50:858–864.
-
Kelsall DR, Lyons TP. Grain dry milling and cooking for alcohol production: designing for 23 percent alcohol production. In: Jacques K, Lyons TP, Kelsall DR, eds. The Alcohol Textbook. 3rd ed. Nottingham, U.K.: Nottingham University Press; 1999:7–24.
-
Kelsall DR, Lyons TP. Grain dry milling and cooking procedures: extracting sugars in preparation for fermentation. In: Jacques KA, Lyons TP, Kelsall DR, eds. The Alcohol Textbook. 4th ed. Nottingham, U.K.: Nottingham University Press; 2003:11.
-
Kelsall DR, Piggott R. Grain dry milling and cooking for alcohol production: designing for the options in dry milling. In: Ingledew WM, Kelsall DR, Austin GD, Kluhspies C, eds. The Alcohol Textbook. 5th ed. Nottingham, U.K.: Nottingham University Press; 2009:161–175.
-
Kindred DR, Verhoeven TMO, Weightman RM, Swanston JS, Agu RC, Brosnan JM, Sylvester-Bradley R. Effects of variety and fertiliser nitrogen on alcohol yield, grain yield, starch and protein content, and protein composition of winter wheat. Journal of Cereal Science. 2008;48:46–57.
-
Lea, A., 2001. There’s something about Riband. Arable Farming, May 26, p. 29.
-
Lineback DR, Rasper VF, Wheat carbohydrates. Pomeranz Y, ed. Wheat Chemistry and Technology, 1. St. Paul, MN: American Association of Cereal Chemists; 1988:277–372.
-
Lynn A, Prentice RDM, Cochrane MP, Cooper AM, Dale F, Duffus CM, Ellis RP, Morrison IM, Paterson L, Swanston JS, Tiller SA. Cereal starches: properties in relation to industrial use. In: Campbell GM, Webb C, McKee SL, eds. Cereals: Novel Uses and Processes. New York: Plenum Press; 1997:69–79.
-
Lynn A, Smith R, Cochrane MP, Sinclair K. Starch granule enzymic digestion. In: Campbell I, ed. Proceedings of the Fifth Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1999:46–54.
-
Lyons TP. Thinking outside the box: ethanol production in the next millennium. In: Jacques K, Lyons TP, Kelsall DR, eds. The Alcohol Textbook. 3rd ed. Nottingham, U.K.: Nottingham University Press; 1999:1–6.
-
MacGregor AW. Starch degrading enzymes. Ferment. 1991;4:178–182.
-
MacGregor AW, Bhatty RS, eds. Barley: Chemistry and Technology. St. Paul, MN: American Association of Cereal Chemists; 1993.
-
MacGregor AW, Fincher GB. Carbohydrates of the barley grain. In: MacGregor AW, Bhatty RS, eds. Barley: Chemistry and Technology. St. Paul, MN: American Association of Cereal Chemists; 1993:73–130.
-
MacGregor AW, Bazin SL, Macri LJ, Babb JC. Modelling the contribution of alpha amylase, beta amylase and limit dextrinase to starch degradation during mashing. Journal of Cereal Science. 1999;29:161–169.
-
MAGB., 2008. Assured UK Malt Manual: The Assured UK Malt Technical Standard, Version 3.4, January. Maltsters Association of Great Britain, Newark (www.ukmalt.com).
-
MAGB Institute of Brewing and Distilling Approved List, Harvest 2013. Newark: Maltsters Association of Great Britain; 2014:(www.ukmalt.com).
-
Miles MJ, Morris VJ, Ring SG. Gelation of amylose. Carbohydrate Research. 1985;135:257–269.
-
Miles MJ, Morris VJ, Orford PJ, Ring SG. The roles of amylose and amylopectin in the gelation and retrogradation of starch. Carbohydrate Research. 1985;135:271–281.
-
Mlotkiewicz JA. The role of the Maillard reaction in the food industry. In: O’Brien J, Nursten HE, Crabbe MJC, Ames JM, eds. The Maillard Reaction in Foods and Medicine. Cambridge, U.K.: Royal Society of Chemistry; 1998:19–27.
-
Muller R. The effects of mashing temperature and mash thickness on wort carbohydrate composition. Journal of the Institute of Brewing. 1991;97:85–92.
-
Newton J, Stark JR, Riffkin HL. The use of maize and wheat in the production of alcohol. In: Campbell I, Priest FG, eds. Proceedings of the Fourth Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1995:189–192.
-
Nicol DA. Developments in distillery practices in response to external pressures. In: Campbell I, ed. Proceedings of the Third Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1990:117–137.
-
O’Brien J, Nursten HE, Crabbe MJC, Ames JM, eds. The Maillard Reaction in Foods and Medicine. Cambridge, U.K: Royal Society of Chemistry; 1998.
-
O’Rourke T. Mash separation systems. The Brewer International. 2003;3(2):57–59.
-
Orth RA, Shellenberger JA, Origin, production and utilization of wheat. Pomeranz Y, ed. Wheat: Chemistry and Technology, 1. St. Paul, MN: American Association of Cereal Chemists; 1988:1–14.
-
Palmer GH. Adjuncts in brewing and distilling. In: Campbell I, Priest FG, eds. Proceedings of the Second Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1986:24–45.
-
Palmer GH. Cereals in malting and brewing. In: Palmer GH, ed. Cereal Science and Technology. Aberdeen, Scotland: Aberdeen University Press; 1989:61–242.
-
Palmer I. Building a brand new grain whisky distillery. Brewer and Distiller International. 2012;8(12):18–23.
-
Pearson T, Wilson J, Gwirtz J, Maghirang E, Dowell F, McCluskey P, Bean S. Relationship between single wheat kernel particle-size distribution and Perten SKCS 4100 hardness index. Cereal Chemistry. 2007;84(6):567–575.
-
Pérez S, Bertoft E. The molecular structures of starch components and their contribution to the architecture of starch granules: a comprehensive review. Starch/Stärke. 2010;62:389–420.
-
Petersen PB, Munck L. Whole crop utilization of barley, including potential new uses. In: MacGregor AW, Bhatty RS, eds. Barley: Chemistry and Technology. St. Paul, MN: American Association of Cereal Chemists; 1993:437–474.
-
Piggott JR, Conner JM. Whiskies. In: Lea AGH, Piggott JR, eds. Fermented Beverage Production. Glasgow: Chapman & Hall; 1995:247–274.
-
Piggott JR, Sharp R, Duncan REB, eds. The Science and Technology of Whiskies. Harlow: Longman Scientific & Technical; 1989.
-
Pomeranz Y, Chemical composition of cereal structures. Pomeranz Y, ed. Wheat Chemistry and Technology, 1. St. Paul, MN: American Association of Cereal Chemists; 1988:97–158.
-
Pyke M. The manufacture of grain whisky. Journal of the Institute of Brewing. 1965;71:209–218.
-
Rae WD. Sustainability in the cereals supply chain. In: Bryce JH, Piggott JR, Stewart GG, eds. Distilled Spirits: Production, Technology and Innovation. Nottingham, U.K.: Nottingham University Press; 2008:2–6.
-
Rankin WD. New production methods in distilling. The Brewer. 1977;63:90–95.
-
Rankin WD. Future trends in plant for maltings breweries and distilleries. In: Campbell I, ed. Proceedings of the Third Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1990:138–148.
-
Riffkin HL, Bringhurst TA, McDonald AML, Hands E. Quality requirements of wheat for distilling. Aspects of Applied Biology. 1990;25:29–40.
-
Robson F. Cameronbridge: a distilling giant. The Brewer International. 2001;1(4):16–19.
-
Robson F. Roof with a view. The Brewer International. 2002;2(1):42–47.
-
Robyt JF. Enzymes in the hydrolysis and synthesis of starch. In: Whistler RL, BeMiller JN, Paschall EF, eds. Starch: Chemistry and Technology. 2nd ed. London: Academic Press; 1984:87–123.
-
SAC SAC Cereal Recommended List for 2012. Edinburgh: Scottish Agricultural College; 2012:(www.sruc.ac.uk).
-
Sasaki T, Yasui T, Matsuki J. Effect of amylose content on gelatinization and pasting properties of starches from waxy and non-waxy wheat and their seeds. Cereal Chemistry. 2000;77:58–63.
-
Shannon JC, Garwood DL. Genetics and physiology of starch development. In: Whistler RL, BeMiller JN, Paschall EF, eds. Starch : Chemistry and Technology. 2nd ed. London: Academic Press; 1984:25–86.
-
Stark WH, Kolachov P, Willkie HF. Wheat as a raw material for alcohol production. Industrial and Engineering Chemistry. 1943;35(2):133–137.
-
Statutory Instrument 2009., 2009. Scotch Whisky Regulations 2009 (Citation 2009, No. 2890). HMSO, London.
-
Stenholm K. Malt Limit Dextrinase and its Importance in Brewing. Espoo, Finland: VTT Publications; 1997.
-
Sun Z, Henson CA. Extraction of α-glucosidase from germinated barley kernels. Journal of the Institute of Brewing. 1992;98:289–292.
-
SWA Scotch Whisky Industry Environmental Strategy Report 2012. London: Scotch Whisky Association; 2012:(www.scotch-whisky.org.uk).
-
Swanston JS, Thomas WTB, Powell W, Young GR, Lawrence PE, Ramsay L, Waugh R. Using molecular markers to determine barleys most suitable for malt whisky distilling. Molecular Breeding. 1999;5:103–109.
-
Swanston JS, Smith PL, Gillespie TL, Brosnan JM, Bringhurst TA, Agu RC. Associations between grain characteristics and alcohol yield among soft wheat varieties. Journal of the Science of Food and Agriculture. 2007;87:676–683.
-
Swinkels JJM. Sources of starch its chemistry and physics. In: Van Beynum GMA, Roels JA, eds. Starch Conversion Technology. New York: Marcel Dekker; 1985:15–46.
-
Sylvester-Bradley, R, Kindred, D, Weightman, R, Thomas, WTB, Swanston, JS, et al. (2010). Genetic Reduction of Energy Use and Emissions of Nitrogen through Cereal Production: GREEN Grain, HGCA Project Report No. 468. Home Grown Cereals Authority, Agriculture and Horticulture Development Board, Kenilworth, U.K.
-
Taylor BR, Roscrow JC. Factors affecting the quality of wheat grain for distilling in Northern Scotland. Aspects of Applied Biology. 1990;25:183–191.
-
Tester RF. Properties of damaged starch granules: composition and swelling properties of maize, rice, pea and potato fractions in water at various temperatures. Food Hydrocolloids. 1997;1:293–301.
-
Travis GL. American bourbon whiskey production. Ferment. 1998;11:341–343.
-
Uthayakumaran S, Wrigley CW. Wheat: characteristics and quality requirements. In: Wrigley CW, Batey IL, eds. Cereal Grains, Assessing and Managing Quality. Cambridge, U.K.: Woodhead Publishing; 2010:59–111.
-
Walker EW. Grain spirit—which cereal? In: Campbell I, Priest FG, eds. Proceedings of the Second Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1986:375–380.
-
Walker, GM and Hughes PS, Eds., 2010. Distilled Spirits. Vol. 3. New Horizons: Energy, Environment and Enlightenment. Nottingham University Press, Nottingham, U.K.
-
Walker GM, Goodall I, Fotheringham R, Murray D, eds. Distilled Spirits: Science and Sustainability. Nottingham, U.K: Nottingham University Press; 2012.
-
Walker JW, Bringhurst TA, Broadhead AL, Brosnan JM, Pearson SY. The survival of limit dextrinase during fermentation in the production of scotch whisky. Journal of the Institute of Brewing. 2001;107(2):99–106.
-
Wan Y, Poole RL, Huttly AK, Toscano-Underwood C, Feeney K, et al. Transcriptome analysis of grain development in hexaploid wheat. BMC Genomics. 2008;9:121.
-
Weightman, R, Sylvester Bradley, R, Kindred, D, and Brosnan, J (2010). Growing Wheat for Alcohol/ Bioethanol Production, HGCA Information Sheet 11. Home Grown Cereals Authority, Agriculture and Horticulture Development Board, Kenilworth, U.K.
-
Whistler RL, BeMiller JN, Paschall EF. Starch: Chemistry and Technology. 2nd ed. London: Academic Press; 1984.
-
Whitby BR. Designing a distillery for the future. In: Campbell I, Priest FG, eds. Proceedings of the Fourth Aviemore Conference on Malting, Brewing and Distilling. London: Institute of Brewing; 1995:100–111.
-
Wilkin GD. Raw materials: milling, mashing and extract recovery. In: Priest FG, Campbell I, eds. Current Developments in Malting Brewing and Distilling. London: Institute of Brewing; 1983:35–44.
-
Wilkin GD. Milling cooking and mashing. In: Piggott JR, Sharp R, Duncan REB, eds. The Science and Technology of Whiskies. Harlow: Longman Scientific & Technical; 1989:64–88.
-
Wrigley CW, Bietz JA, Proteins and amino acids. Pomeranz Y, ed. Wheat Chemistry and Technology, 1. St. Paul, MN: American Association of Cereal Chemists; 1988:201.
-
Zobel HF. Gelatinization of starch and mechanical properties of starch pastes. In: Whistler RL, BeMiller JN, Paschall EF, eds. Starch: Chemistry and Technology. 2nd ed. Orlando, FL: Academic Press; 1984:285–309.
下一章:第7章:酿造酵母与发酵